置换反应是无机化学反应的基本类型之一,指一种单质和一种化合物生成另一种单质和另一种化合物的反应。
置换反应的定义_置换反应 -简介
置换反应(displacement reaction)是无机化学反应的四大基本反应类型之一,指一种单质和一种化合物生成另一种单质和另一种化合物的反应,可表示为:A+BC=B+AC 或 AB+C=AC+B
除此之外,也可以指路易斯酸间的置换反应,此时并不需要单质参与反应。出处是高等教育出版社的《无机化学》(第四版)下册第460页正文第3行:“……能将另一个较弱的路易斯酸MnF4从稳定配离子[MnF6] 2-的盐中置换出来”?
置换关系是指组成化合物的某种元素被组成单质的元素所替代。
置换反应一定是氧化还原反应,而氧化还原反应不一定是置换反应。
置换反应的定义_置换反应 -分类
一、根据反应环境分类
根据反应环境的类别,置换反应有以下2种情况:
(1)干态置换在加热或高温条件下固体与固体或固体与气体发生的置换反应。
(2)湿态置换 在水溶液中进行的置换反应。
①金属跟酸的置换
是金属原子与酸溶液中氢离子之间的反应。
要特别注意不能用浓硫酸,硝酸,它们有强氧化性,先将金属氧化成对应氧化物,氧化物再溶于酸中,然后继续氧化,继续溶解,反应得以继续
Zn+2HCl====ZnCl2+H2↑
Zn+H2SO4(稀)====ZnSO4+H2↑
2Al+3H2SO4(稀)====Al2(SO4)3+3H2↑
2.金属跟盐溶液的置换
是金属原子跟盐溶液中较不活泼金属的阳离子发生置换。如:
Cu+Hg(NO3)2====Hg+Cu(NO3)2
二、根据元素性质分类
按元素的性质划分,金属与非金属单质间的置换。
1.金属单质置换金属单质
2Al+Fe2O3=高温=Al2O3+2Fe (铝热反应。Al还可与V2O5.CrO3.WO3.MnO2等发生置换)
Fe+CuSO4=FeSO4+Cu
2.金属单质置换非金属单质
Zn+2HCl=H2↑+ZnCl2
2Na+2H2O=2NaOH+H2 ↑
2Mg+CO2=点燃=2MgO+C
3Fe+4H2O(g)=高温=Fe3O4+4H2
4Na+3CO2=点燃=2Na2CO3+C
3.非金属单质置换金属单质
H2+CuO=Δ=Cu+H2O
C+FeO=Δ=Fe+CO↑
Si+2FeO=Δ=2Fe+SiO2
C+2CuO=高温=2Cu+CO2↑
4.非金属单质置换非金属单质
2F2+2H2O=4HF+O2
2C+SiO2=Si+2CO ↑
C+H2O=高温=CO+H2
2H2+SiCl4=Si+4HCl
Cl2+2NaBr=Br2+2NaCl
O2+2H2S=2S↓+2H2O
Br2+2HI=2HBr+I2
三、根据元素周期表中位置分类
按元素在周期表的位置划分,同族元素单质间的置换与不同族元素单质间的置换。
1.同主族元素单质间的置换
Na+KCl=高温=NaCl+K↑(一般是774℃)
2Na+2H2O=2NaOH+H2↑
2H2S+O2=2S+2H2O
2C+SiO2=Si+2CO↑
F2+2HCl=2HF+Cl2
2.不同主族元素单质间的置换
Mg+2HCl=MgCl2+H2↑
2Mg+CO2=2MgO+C
2Al+6HCl=2AlCl3+3H2↑
2F2+2H2O=4HF+O2
C+H2O(g)==高温==CO+H2
2H2+SiCl4=Si+4HCl
H2S+Cl2=S+2HCl
3Cl2+8NH3=6NH4Cl+N2
4NH3+3O2==点燃==2N2+6H2O (氨气在纯氧中燃烧)
3.主族元素单质置换副族元素的单质
H2+CuO=Cu+H2O
2Al+Fe2O3=Al2O3+2Fe
C+CuO=Cu+CO
2Al+3Hg2+=2Al3++3Hg
4Na+TiCl4=4NaCl+Ti
4.副族元素的单质置换主族元素单质
3Fe+4H2O(g)==加热==Fe3O4+4H2
Zn+2H+=Zn2++H2
5.副族元素的单质置换副族元素的单质
Fe+CuSO4=FeSO4+Cu
四、根据物质类别分类
按物质类别划分,单质与氧化物间的置换和单质与非氧化物间的置换。
1.单质与氧化物发生置换反应
2Na+2H2O=2NaOH+H2↑
2Mg+CO2=点燃=2MgO+C
3Fe+4H2O=Fe3O4+4H2
H2+CuO=Δ=Cu+H2O
C+FeO=高温=Fe+CO↑
2F2+2H2O=4HF+O2
2C+SiO2=Si+2CO↑
2Al+Fe2O3=Al2O3+2Fe
C+H2O(g)=高温=CO+H2
Si+2FeO=2Fe+SiO2
3H2+Fe2O3=Δ2Fe+3H2O
2.单质与非氧化物发生置换反应
2H2+SiCl4=Si+4HCl
H2S+Cl2=S+2HCl
3Cl2+8NH3=6NH4Cl+N2
4NH3+3O2=2N2+6H2O
Mg+2HCl=MgCl2+H2
2Al+6HCl=2AlCl3+3H2
湿态置换遵守金属活动性顺序。
置换反应不一定为氧化还原反应,氧化还原反应一定为置换反应。
另外需要注意的是置换反应是根据金属活泼性顺序表发生的。
五、金属活动性顺序表
金属活动性顺序表Fr
钫
Cs
铯
Rb
铷
K
钾
Ra
镭
Ba
钡
Sr
锶
Ca
钙
Na
钠
Li
锂
Ac
锕
La
镧
Ce
铈
Pr
镨
Nd
钕
Pm
钷
Sm
钐
Eu
铕
Gd
钆
Tb
铽
Y
钇
Mg
镁
Dy
镝
Am
镅
Ho
钬
Er
铒
Tm
铥
Yb
镱
Lu
镥
H
氢
Sc
钪
Pu
钚
Th
钍
Np
镎
Be
铍
U
铀
Hf
铪
Al
铝
Ti
钛
Zr
锆
V
钒
Mn
锰
Nb
铌
Zn
锌
Cr
铬
Ga
镓
Fe
铁
Cd
镉
In
铟
Tl
铊
Co
钴
Ni
镍
Mo
钼
Sn
锡
Pb
铅
D2
氘分子
H2
氢分子
Cu
铜
Tc
锝
Po
钋
Hg
汞
Ag
银
Rh
铑
Pd
钯
Pt
铂
Au
金初中要求掌握
K
钾
Ca
钙
Na
钠
Mg
镁
Al
铝
Zn
锌
Fe
铁
Sn
锡
Pb
铅
H
氢
Cu
铜
Hg
汞
Ag
银
Pt
铂
Au
金
其中10号氢是过渡元素它前面的可以置换出氢,它后面的则不可以。也就是说氢前面的可以和酸反应生成 氢气,而氢后面的基本不和酸反应就算反应也不生成氢气
置换反应的定义_置换反应 -反应原则
必须是活动性强的金属置换活动性弱的金属溶液
置换反应的定义_置换反应 -相关口诀
钾钙钠镁铝 锌铁锡铅(氢) 铜汞银铂金
(K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au)
以H为标准,(K、Ca、Na、Mg、Al 、Zn、Fe、Sn、Pb)是活泼金属,(Cu、Hg、Ag、Pt、Au)是不活泼金属。
置换反应的定义_置换反应 -反应现象
(1)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)
1、锌和稀硫酸反应:Zn + H2SO4 === ZnSO4 + H2↑
2、镁和稀硫酸反应:Mg + H2SO4 === MgSO4 + H2↑
3、铝和稀硫酸反应:2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑
4、锌和稀盐酸反应:Zn + 2HCl === ZnCl2 + H2↑
5、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑
6、铝和稀盐酸反应:2Al + 6HCl === 2AlCl3 + 3H2↑
16的现象:有气泡产生。
7、铁和稀盐酸反应:Fe + 2HCl === FeCl2 + H2↑
8、铁和稀硫酸反应:Fe + H2SO4 === FeSO4 + H2↑
7-8铁参加的置换反应显+2价,7-8的现象:有气泡产生,溶液由无色变成浅绿色。
(2)金属单质 + 盐(溶液) ---另一种金属 + 另一种盐
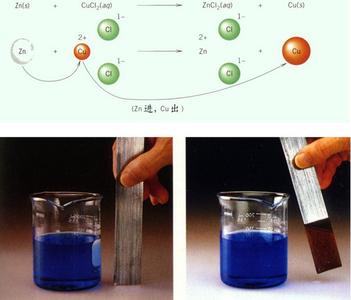
9、铁与硫酸铜反应:Fe+CuSO4 == Cu+FeSO4
现象:铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
(古代湿法制铜及"曾青得铁则化铜"指的是此反应)
10、锌片放入硫酸铜溶液中:CuSO4 + Zn == ZnSO4 + Cu
现象:锌片表面覆盖一层红色的物质,溶液由蓝色变成无色。
11、铜片放入硝酸银溶液中:2AgNO3+Cu==Cu(NO3)2+2Ag
现象:铜片表面覆盖一层银白色的物质,溶液由无色变成蓝色。?
3)金属氧化物+木炭或氢气→金属+二氧化碳或水
12、焦炭还原氧化铁:3C+ 2Fe2O3==高温==4Fe + 3CO2↑冶炼金属
13、木炭还原氧化铜:C+ 2CuO==高温==2Cu + CO2↑冶炼金属
现象:黑色粉末变成红色,澄清石灰水变浑浊。
14、氢气还原氧化铜:H2 + CuO==△==Cu + H2O
现象:黑色粉末变成红色,试管内壁有水珠生成
15、氢气与氧化铁反应:Fe2O3+3H2==△==2Fe+3H2O
16、水蒸气通过灼热碳层:H2O + C==高温==H2 + CO 水煤气的制法
置换反应的定义_置换反应 -置换反应
铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑
镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑
氢气还原氧化铜:H2+CuO加热Cu+H2O
木炭还原氧化铜:C+2CuO高温2Cu+CO2↑
甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O
水蒸气通过灼热碳层:H2O+C高温H2+CO
焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑
 爱华网
爱华网