无机化学是高考必考点。下面是小编为大家整理的2016无机化学知识点高考复习,希望对大家有所帮助。
2016无机化学知识点高考复习(一)1、常见分子(或物质)的形状及键角
(1)形状:V 型:H2O、H2S 直线型:CO2、CS2 、C2H2 平面三角型:BF3、SO3 三角 锥型:NH3 正四面体型:CH4、CCl4、白磷、NH4+ 平面结构:C2H4、C6H6
(2)键角:H2O:104.5°;BF3、C2H4、C6H6、石墨:120° NH3:107°18′
2、常见粒子的饱和结构:
①具有氦结构的粒子(2) :H 、He、Li+、Be2+;
②具有氖结构的粒子(2、8) 3 、O2 、F 、Ne、Na+、Mg2+、Al3+; :N
③具有氩结构的粒子(2、8、8) 2 、Cl 、Ar、K+、Ca2+; :S
④核外电子总数为 10 的粒子: 阳离子:Na+、Mg2+、Al3+、NH4+、H3O+; 阴离子:N3 、O2 、F 、OH 、NH2 ; 分子:Ne、HF、H2O、NH3、CH4
⑤核外电子总数为 18 的粒子: 阳离子:K+、Ca 2+; 阴离子:P3 、S2 、HS 、Cl ; 分子:Ar、HCl、H2S、PH3、SiH4、F2、H2O2、C2H6、CH3OH、N2H4。 3、常见物质的构型: AB2 型的化合物(化合价一般为+2、-1 或+4、-2) :CO2、NO2、SO2、SiO2、CS2、ClO2、 CaC2、MgX2、CaX2、BeCl2、BaX2、KO2 等 A2B2 型的化合物:H2O2、Na2O2、C2H2 等 A2B 型的化合物:H2O、H2S、Na2O、Na2S、Li2O 等 AB 型的化合物:CO、NO、HX、NaX、MgO、CaO、MgS、CaS、SiC 等 能形成 A2B 和 A2B2 型化合物的元素:H、Na 与 O,其中属于共价化合物(液体)的是 H ;属于离子化合物(固体)的是 Na 和 O[Na2O 和 Na2O2]
4、常见分子的极性: 常见的非极性分子:CO2、CS2、BF3、CH4、CCl4、 6、C2H4、C2H2、C6H6 等 、SF 常见的极性分子:双原子化合物分子、H2O、H2S、NH3、H2O2、CH3Cl、CH2Cl2、CHCl3 等
5、一些物质的组成特征:
(1)不含金属元素的离子化合物:铵盐
(2)含有金属元素的阴离子:MnO4 、AlO2 、Cr2O72 (
3)只含阳离子不含阴离子的物质:金属晶体
2016无机化学知识点高考复习(二)1、气体具有两个基本特性:扩散性和可压缩性。主要表现在:
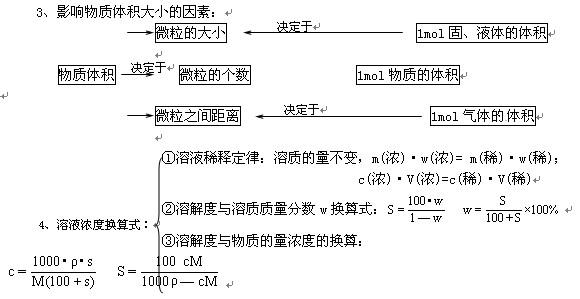
⑴气体没有固定的体积和形状。⑵不同的气体能以任意比例相互均匀的混合。⑶气体是最容易被压缩的一种聚集状态。
2、理想气体方程:PVnRT R为气体摩尔常数,数值为R=8.314Jmol1K1
3、只有在高温低压条件下气体才能近似看成理想气体。
4、当两种或两种以上的气体在同一容器中混合时,每一种气体称为该混合气体的组分气体。
5、混合气体中某组分气体对器壁所施加的压力叫做该组分气体的分压。
6、对于理想气体来说,某组分气体的分压力等于相同温度下该组分气体单独占有与混合气体相同体积时所产生的压力。
7、Dlton分压定律:混合气体的总压等于混合气体中各组分气体的分压之和。
2016无机化学知识点高考复习(三)1、 系统是人们将其作为研究对象的那部分物质世界,即被研究的物质和它们所占有的空间。系统的边界可以是实际的界面也可以是人为确定的用来划定研究对象的空间范围。划定范围的目的是便于研究。
2、 环境是系统边界之外与之相关的物质世界。
3、 系统与环境之间可能会有物质和能量的传递。按传递情况不同,将系统分为:
⑴封闭系统:系统与环境之间只有能量传递没有物质传递。系统质量守恒。
⑵敞开系统:系统与环境之间既有能量传递〔以热或功的形式进行〕又有物质传递。 ⑶隔离系统:系统与环境之间既没有能量传递也没有物质传递。
4、 状态是系统中所有宏观性质的综合表现。描述系统状态的物理量称为状态函数。状态函数的变化量与系统状态的变化途径无关。
5、 当系统的某些性质发生变化时,这种改变称为过程。系统由始态到终态所经历的过程总和被称为途径。
 爱华网
爱华网