判断物质是否电解质的方法
寇介芳
一、电解质和非电解质的概念
电解质:在水溶液中或熔融状态下能导电的化合物。
非电解质:在水溶液中和熔融状态下不能导电的化合物。
注意:
(1)电解质和非电解质都必须是化合物。
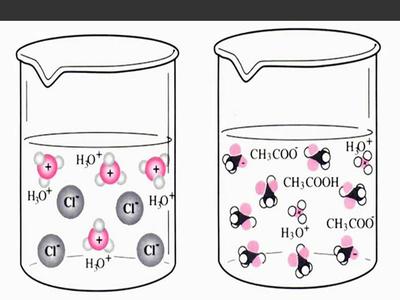
(2)电解质和非电解质都必须是纯净物。
(3)电解质溶液导电必须是自身电离产生自由移动的离子。
(4)电解质与导电性无确定关系。
二、判断方法
根据物质的类别判断。
1.属于电解质的物质
(1)大部分盐,如NaCl、Na2SO4、BaSO4等;
(2)活泼金属的氧化物,如Na2O、Al2O3等;
(3)碱,如NaOH、Ba(OH)2、NH3·H2O等;
(4)酸,如HCl、H2SO4、HNO3、CH3COOH、H2CO3等;
(5)水。
2.属于非电解质的物质
(1)非金属氧化物,如CO2、SO2、SO3等;
(2)大部分有机物,如乙醇、蔗糖、CH4等;
(3)少数非金属氢化物,如NH3。
三、例题与练习
1.下列说法正确的是()
A.将BaSO4放入水中不能导电,所以BaSO4是非电解质
B.NH3的水溶液能导电,所以NH3是电解质
C.硫酸是电解质,所以稀硫酸和熔融态的硫酸都能导电。
D.NaCl是电解质,固体NaCl不导电,熔融态的NaCl能导电
答案:D。
2.下列常见物质中:
① BaSO4固体②液态HCl ③Al2O3④铜棒
⑤饱和食盐水⑥液态SO3⑦氨水
⑧ Ba(OH)2 ⑨熔融的KNO3⑩酒精
(1)属于电解质的物质是;
(2)属于非电解质的物质是;
(3)能导电的物质是;
(4)除⑤⑦之外的物质中,溶于水后能导电的是。
答案:(1)①②③⑧⑨(2)⑥⑩
(3)④⑤⑦⑨(4)②⑥⑧⑨
四、小结
1.电解质和非电解质都是化合物,如Cl2、Cu等单质;
2.电解质和非电解质都是纯净物,如盐酸、食盐水等溶液;
3.电解质不一定能导电,如NaCl晶体、BaSO4溶液等;
4.能导电的物质不一定是电解质,如铁、氯水、氨水等;
5.电解质在熔融状态下不一定能导电,如熔融的H2SO4等。
 爱华网
爱华网