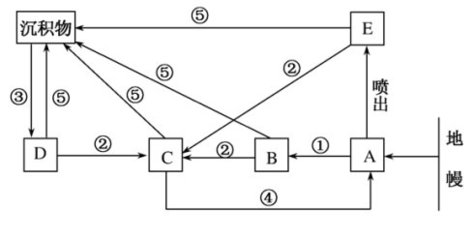
一轮复习检测计算题
1.在一烧杯中盛有11.4g Na2CO3和Na2SO4组成的固体混合物,加94g水溶解,制成溶液。向其中逐渐滴加溶质质量分数为20%的稀硫酸,放出气体的总质量与所滴入稀硫酸的质量关系曲线如图所示:请根据题意回答问题:
(1)当滴加了49g稀硫酸时,放出气体的总质量为g。
(2)当滴加稀硫酸至图中B点时,烧杯中溶液里的溶质是(写化学式)。
(3)当滴加了49g稀硫酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
【答案】
(1)4.4g
(2)Na2SO4H2SO4
(3)11.4g-10.6g+14.2g=15g
2.在一烧杯中盛有MgCO3和MgCl2的粉末状混合物,加入质量分数为7.3%的稀盐酸至恰好完全反应,得到150g不饱和溶液,然后向该溶液中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示。请根据题意回答下列问题:
⑴在滴入稀盐酸的过程中,观察到的明显现象是:
①________________,②___________________。
⑵当滴入10%的氢氧化钠溶液至图中B点时,烧杯中溶液里含有的溶质是(写化学式)_______________。
⑶当滴入10%的氢氧化钠溶液40g时(即A点),试通过计算,求此时烧杯中所得不饱和溶液的质量。
(计算结果精确到0.1g)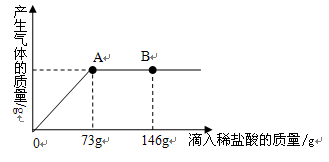
【答案】
(1)固体逐渐消失,有气体产生
(2)NaClMgCl2
(3)150g+40g-2.9g=187.1g
3.在一烧杯中盛有30.8gBaCO3和BaCl2的粉末状混合物,向其中加入200g水,使混合物中的可溶物完全溶解。然后再向其中逐滴加入溶质的质量分数为10%的稀盐酸,产生气体的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:
⑴在滴入稀盐酸的过程中,观察到的明显现象是:①_______________,②_____________。
⑵当滴入10%的稀盐酸至图中B 点时,烧杯中溶液里含有的溶质是(写化学式)_______。
⑶当滴入10%的稀盐酸73g时(即A点),试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量。(计算结果精确到0.1g)
【答案】
(1)难溶物逐渐消失; 有气体产生
(2)BaCl2HCl
(3)30.8g-19.7g+20.8g=31.9g
4. 在一烧杯中盛有一定质量的Na2CO3和Na2SO4固体,加入一定量的水制成150g不饱和溶液,向其中滴加溶质的质精分数为9.8%的H2SO4溶液,产生气体的质量与所滴入H2SO4溶液的质量关系曲线如图所示。请根据题意回答下列问题:
(1)在滴入稀硫酸时,观察到的明显实验现象是____________________________。
(2)当滴入H2SO4溶液至图中B点时,烧杯中溶液里含有的溶质是(写化学式)______。
(3)当滴入9.8%的H2SO4溶液20g时(即A点),试通过计算,求此时所得不饱和溶液中溶液的质量。(计算结果精确至0.1g)
(1)有气体产生 (2)H2SO4Na2SO4 (3)100g+20g-0.88g=119.1g |
【友情提示】溶液质量的计算最好根据质量守恒来进行计算,用放入烧杯内物质的总质量-反应后不属于溶液的质量(不属于溶液的部分包括气体、沉淀、不溶性杂质)
也就是说,拿到题目,看到要求溶液质量时,就要求气体、沉淀、不溶性杂质的质量。
 爱华网
爱华网