2011.04.1后进口非特殊用途化妆品在申报I注册备案药监局批文的资料要求增加了一些内容,但网络上的信息都并没有及时更新,现我北京曼莫尔公司特此撰文编写一套完整的申报资料及申报流程方案.
一、授权书备案
1. 授权书应由化妆品生产企业和行政许可在华申报责任单位双方共同签署
2.化妆品生产企业负责人签字或盖章均可,行政许可在华申报责任单位应由法定代表人签字和盖章,并经公证机关公证;授权书为外文的,还应译成中文,并对中文译文公证。
3.授权书应包括以下内容:授权单位名称地址、行政许可在华申报责任单位名称地址、授权有效期(至少四年)、所授权的产品范围、授权权限等;授权权限应包括委托行政许可在华申报责任单位代理申报,还可以包括代表化妆品生产企业加盖印章确认申报资料,
4.应提交授权书原件(包括中文译文)存档备查。
5.办理有关进口化妆品或进口化妆品新原料行政许可事项申请受理业务时,具体办事人员应提交在华申报责任单位的办事委托书及相关证件。
二、检验
1.进口非特殊类化妆品在申报药监局(08年9月份化妆品申报由卫生部卫生监督中心划入国家药监局)之前先要送到国家指定的检验机构进行检验。送检时提供配方、说明书、及样
品。样品具体数量根据产品的规格来定,一般是12瓶左右,如有加测的检验项目如另算,如乙醇超10%、二噁烷、苯酚、宣传祛痘、抗粉刺等功效都要另外加测项目。
2.注意:在提供样品的时候请注意一定要是未开封的市售包装,为了保证产品检验的合格。![[转载]进口非特殊用途化妆品申报注册流程及申报资料要求 特殊用途化妆品](http://img.413yy.cn/images/31101031/31015030t01edc2f6c9ad973650.jpg)
3.检验时间,我公司有长期合作的检验机构,时间方面会比一般规定的时间要快一段时间,一般是在1个半月(是在保证质量的基础上),
(关于具体有哪些检验机构及检验项目,可以参照我发布的《2010年进口化妆品注册申报全程指南》中已经明确列出)
三、资料准备
进口非特殊用途化妆品所需要资料列表如下:
(一)进口非特殊用途化妆品行政许可申请表;
(二)产品中文名称命名依据;
(三)产品配方;
(四)产品质量安全控制要求;
(五)产品原包装(含产品标签、产品说明书);拟专为中国市场设计包装的,需同时提交产品设计包装(含产品标签、产品说明书);
(六)经国家食品药品监督管理局认定的许可检验机构出具的检验报告及相关资料;
(七)产品中可能存在安全性风险物质的有关安全性评估料;
(八)已经备案的行政许可在华申报责任单位授权书复印件及行政许可在华申报责任单位营业执照复印件并加盖公章;
(九)化妆品使用原料及原料来源符合疯牛病疫区高风险物质禁限用要求的承诺书;
(十)产品在生产国(地区)或原产国(地区)生产和销售的证明文件;
(十一)授权书;
(十二)产品生产工艺流程图及简述
(十三)化妆品技术要求
另附疾控中心封样的样品1件
以上资料可以在做检验的同时准备完成。但是授权书必须在检验前备案,只有授权书备案通过了,才能提交其他的申报材料。授权书做起来是非常麻烦的,需要公证的内容比较多,有几个要点是非常重要的,如授权国内在华责任单位为经销商或代理商及在华责任单位,负责产品的申报注册事宜,授权期限,授权范围。我公司有固定的样本,可以提供给客户,并指导客户来去做一些公证的事情。
以上资料看似简单,但在准备时有很多细节性的东西在里面,比如配方是最重要的,所以配方的审核比较重要,并不是说做化妆品研发的人就看过后就一定没有问题,主要是要符合国家的规定。而有些规定是没有成文的,所以就要靠经验。我公司为客户提供先审配方后签合同的服务,保障客户的利益。
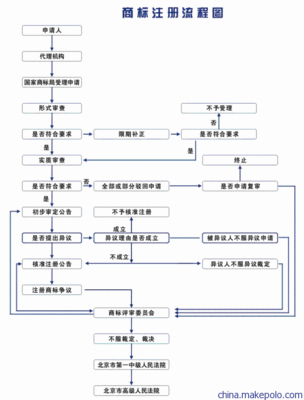
四、申报药监局备案
在申报药监局备案时要将以上资料装订成册,前自送往药监局,5个工作日后如有问题需要补充,会出补正意见,要求企业进行补充,如果没有问题即可受理,受理后专家会对产品进行评审,一般在20个工作日之内,评审完成后,如有问题,即出不予批准建议书,告知企业问题所在,如企业觉得专家提出的意见不合理,可提出复核申请,将自己的理由递交
给评审中心。接受后90个工作日内会给予答复(时间很漫长),如果评审后没有问题,即转入国家药监局总局会再进行复审,审核通过即可领导签字,制证发证,一般在20个工作日左右。
所以,进口非特殊用途化妆品从检验到拿证一般是在4个月左右,这是在非常顺利的前提下。
以上内容仅做为参考,如读者对以上内容有疑问可随时与本公司联系。为客户把问题解决在申报之前。
 爱华网
爱华网