喷泉实验的原理及其考查题型
1.形成原因:P(外)≠P(内)
2.形成条件:气体极“易”“溶”于“溶剂”
易:溶解度大且溶解速度快
溶:可是物理过程,也可是发生化学反应导致气体的消耗
溶剂:可是水,也可以是某种溶液
3.常见实例:
水作溶剂:HCl、HBr、HI、SO2、NH3…
NaOH溶液作溶剂:H2S、CI2、CO2以及易溶于水的气体HCl、HBr、HI、SO2、NH3…
二,喷泉实验的考查方式:
题型一:引发方式
1.使烧瓶内部压强减小,外部压强不变。(图1)
2.使烧瓶内部压强不变,外部压强增加大。(图2)
例题1:喷泉是一种常见的自然现象,其产生原因是存在压强差。
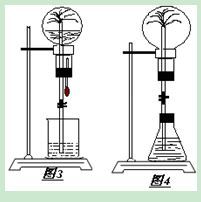
(1)图3为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是( B)
A、HCI和H2OB、O2和H2O
C、NH3和H2OD、CO2和NaOH溶液
(2)某学生积极思考产生喷泉的其他办法,并设计了如图所示的装置。
①在图4的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是(D)
A、Cu和稀盐酸B、NaHCO3与NaOH溶液
C、CaCO3与稀盐酸D、NH4HCO3与稀盐酸
②在图4的锥形瓶外放一水槽,瓶中加入酒精,水槽中加入冰水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质是:(A)
A、浓硫酸B、食盐C、硝酸钾D、硫酸铜
这种方法产生喷泉的原理是: 浓硫酸溶解放出大量的热是酒精大量挥发,产生的压力应该,引发喷泉。
③比较图3和图4两套装置,从产生喷泉的原理来分析,图3是减少上部烧瓶内气体压强,图4题增大 下部锥形瓶内气体压强(均填“增大”或“减小”)
(3)城市中常见的人造喷泉及火山爆发的原理与上述图4(填图3或图4装置的原理相似)
题型二:形成根本原因与美丽的颜色
例题2:喷泉是一种优美的自然现象,在实验室可根据某些物质的性质进行模拟。
编号 | 烧瓶中 气体 | 烧杯中的液体 | 喷泉的颜色 | 变色的原因 |
1 | HCl | 石蕊试液 | 红色 | HCl的水溶液呈酸性,遇石蕊试液变红 |
硝酸银溶液 | 白色 | 产生了白色的AgNO3沉淀 | ||
氢氧化铜悬浮液 | 绿色 | 2HCl+Cu(OH)2=CuCl2+2H2O,在CuCl2的水溶液中存在[CuCl4]2-和[Cu(H2O)4]2+两种绿色离子 | ||
2 | Cl2 | KSCN的FeCl2溶液 | 红色 | Cl2氧化Fe2+变为Fe3+,使KSCN变红 |
KI的淀粉溶液 | 蓝色 | Cl2置换出KI中的I2,I2与淀粉变蓝 | ||
KBr的CCl4溶液 | 橙色 | Cl2置换出KBr中的Br2,Br2的CCl4溶液呈橙色 | ||
3 | NH3 | 酚酞试液 | 红色 | NH3的水溶液呈碱性,遇酚酞变红 |
石蕊试液 | 蓝色 | NH3的水溶液呈碱性,遇石蕊变蓝 | ||
FeCl3溶液 | 红褐色 | 产生了红褐色的Fe(OH)3沉淀 | ||
4 | CO2 | 酚酞NaOH溶液 | 透明 | CO2与NaOH产生Na2CO3,使酚酞褪色 |
紫色石蕊试液 | 红色 | CO2的水溶液呈酸性,遇石蕊试液变红 | ||
澄清石灰水 | 白色 | 产生了白色碳酸钙沉淀 |
题型三:喷泉实验后溶液的浓度。
例三:求下列气体作喷泉实验后溶液的浓度之比(相同条件下)
1,NH3和H2O充满烧瓶2,HCl和H2O充满烧瓶
3,HCl和H2O充满烧瓶的三分之二4,NO2与O2按4:1和H2O
5,NO与O2按4:3和H2O6,NO2和H2O
7,装满NO或NO2的试管中通O2至充满液体
 爱华网
爱华网