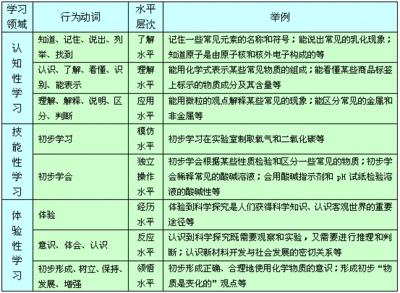
(1)有关质量分数的计算(用两种不同浓度溶液的质量分数与混合溶液的质量分数作十字交叉,求两种溶液的质量比)
(2)有关物质的量浓度的计算(用混合钱的物质量的浓度与混合后的物质量的浓度做十字交叉,求体积比)
(3)有关平均分子量的计算(通过纯物质的物质量分数与混合后的平均分子量做十字交叉,求百分数)
(4)有关平均原子量的计算(用同位素的原子量或质量数与元素原子量作交叉,求原子个数比或同位素百分数)
(5)有关反应热的计算(有单个反应的热效应与混合都反应热做十字交叉,求百分数)
(6)有关混合物反应的计算(利用单个反应消耗某种反应物的量与混合后做十字交叉,求分数)
(7)相关结构的推测(找到相对应的比例关系,如点,边,面等的关系,在做交叉,球分数)
(8)有关体积分数的测定(用组分的式量与混合气的平均式量做十字交叉,求组分体积比或含量)
(9)有关两种含相同元素物质的质量比(用两种物质中同一元素的质量分数求两物质的质量比)
有以下几道例题来分别对这几点的应用作解释(一~六题转载自http://www.xici.net/b346440/d19148200.htm
)
一.有关质量分数的计算:
例: 实验室用密度为1.84克/厘米3 98%的浓硫酸与密度为1.1克/厘米3 15%的稀硫酸混和配制密度为1.4克/厘米359%的硫酸溶液, 取浓、稀硫酸的体积比最接近的值是
A. 1:2 B. 2:1 C. 3:2 D. 2:3
[分析] 98 44
59 /
/ 其体积比为: 44/1.84 : 39/1.1 ≈ 2:3
15 39 答案为 D
根据溶质质量守恒, 满足此式的是98%X + 15% Y = 59%(X+Y)
X 和 Y 之比是溶液质量比,故十字交叉得出的是溶液质量比为44 : 39 ,再换算成体积比
二.有关物质的量浓度的计算
例: 物质的量分别为6摩/升, 1摩/升的硫酸溶液,按怎样的体积比才能配成4摩/升的 溶液?
[分析] 6 3
4 /
/
1 2
根据溶质物质的量守恒, 满足此式的是6X + Y = 4 (X+Y)
X 和 Y 之比是体积比,故十字交叉得出的是体积比为3 : 2 ,答案为6摩/升, 1摩/升的硫酸溶液,按3 :2的体积比才能配成4摩/升的溶液?
三. 有关平均分子量的计算
例: 实验测得乙烯与氧气混合气体的密度是氢气的14.5倍,可知其中乙烯的质量百分比为:
A.25.0% B.27.6% C.72.4% D.75.0%
[分析] 28 3
29 /
/
32 1
根据质量守恒, 满足此式的是 28X + 32 Y = 29(X+Y)
X 和 Y 之比是物质的量之比,故十字交叉得出的是物质的量比3 : 1,
3×28
乙烯的质量百分含量= ------------------ ×100% = 72.4 % 答案为C
3×28+1×32
四. 有关平均原子量的计算
例: 铜有两种天然同位素 63Cu和 65Cu , 参考铜的原子量为63.5 , 估算 63Cu 的平均原子百分含量约是
A. 20% B.25% C.66.7% D.75%
[分析] 63 1.5
63.5 /
/
65 0.5
根据质量守恒, 满足此式的是 63X + 65 Y = 63.5 (X+Y)
可知X :Y 应为原子个数比,故十字交叉法得出的是原子个数比.
1.5
故 63Cu的原子百分含量= ---------×100% =75%
1.5 + 0.5
五. 有关反应热的计算
例: 已知下列两个热化学方程:2H 2(气) + O2 (气) = 2H2 O(液) +571.6千焦
C3H8 (气) +5O2 (气) = 3CO2 (气) + 4H2O (液) + 2220千焦,实验测知氢气和丙烷的混和气体共5摩尔完全燃烧时放热3847千焦, 则混和气体中氢气和丙烷的体积比是
A. 1:3 B. 3:1 C.1:4 D. 1:1
[分析] 571.6
-------- 1450.6
2 3847 /
-----
5
/
2220 483.6
根据总热量守恒, 满足此式的是 285.8X + 2220 Y = 769.4 (X+Y)
可知X :Y 应为物质的量比,故十字交叉法得出的是物质的量比, 即体积比
当然本题用估算法更简单.
六. 有关混和物反应的计算
例:已知白磷和氧气可发生如下反应:P4 +3O2 = P4O6 ,P4 +5O2 = P4O10在某一密闭容器中加入62克白磷和50.4升氧气(标准状况), 使之恰好完全反应, 所得到的P4O10 与P4O6的物质的量之比为
A. 1:3 B. 3:2 C. 3:1 D. 1:1
[分析] P4O10 5 1.5
2.25/0.5 /
/
P4O6 3 0.5
根据O2物质的量守恒, 满足此式的是5X + 3Y = 2.25/0.5 (X+Y)
X 和 Y 之比是P4O10 和P4O6物质的量比,故十字交叉得出的物质的量比为3:1, 答案为C
七.相关结构的推测
1996年的诺贝尔化学奖授予对发现C60有重大贡献的三位科学家。C60是由60个C原子组成的分子,它结构为简单多面体形状。这个多面体有60个顶点,从每个顶点引出3条棱,各面的形状分为五边形和六边形两种,计算C60分子中形状为五边形和六边形的面各有多少?
解析:因每两个顶点共有一条棱故每个顶点独立拥有1.5条棱,所以棱数=1.5*60=90
根据欧拉公式:顶点数+面数-棱数=2(Y+F-E=2)
可知C60的面数=2+90-60=32
若此多面体的面全为五边形则应有32*5/3个顶点(一个五边形有5个顶点每个顶点被三个面所共有),同理若全为六边形则应有32*6/3个顶点。
五边形32*5/34
/
/
60
/
/
六边形32*6/320/3 ∴五边形:六边形= 12:20=3:5
∴五边形12个,六边形 20 个。
八.有关体积分数的计算
已知H2 和CO 的混合气,其平均式量是20,求混合气中H2 和CO 的体积比。(4∶9)
解:H2228-204
╲ ╱
—— 20——
╱ ╲
CO2820-29
九.有关两种含相同元素物质的质量比
FeO 中和FeBr2 的混合物中Fe 的质量百分率为50%,求两物质的质量比(13∶15)
解:FeO7/913/5413
╲ ╱
——1/2——
╱ ╲
FeBr27/275/1815
 爱华网
爱华网