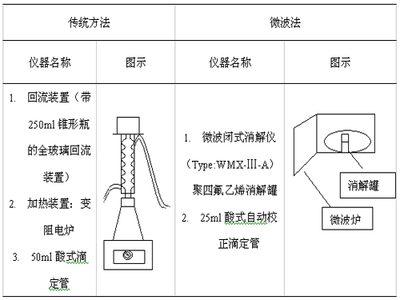
重铬酸钾法(Potassium DichromateMethod):以重铬酸钾K2Cr2O7为滴定剂的方法,是氧化还原滴定法中的重要方法之一。在水质分析中常用于测定水中的化学需氧量(简称COD)。
8.1.1.1重铬酸钾的特性
重铬酸钾K2Cr2O7,橙红色晶体,溶于水。它的主要特点如下。
1.K2Cr2O7固体试剂易纯制并且稳定。在120℃时2~4h,可直接配制标准溶液,而不需标定。
2.K2Cr2O7标准溶液非常稳定,只要保存在密闭容器中,浓度可长期保持不变。
3.滴定反应速度较快,通常可在常温下滴定,一般不需要加入催化剂。
4.需外加指示剂,滴定过程中,Cr2O72-被还原为绿色的Cr3+,但因K2Cr2O7溶液浓度不是很深,所以不能根据自身颜色的变化来确定滴定终点,而要外加指示剂。如用K2Cr2O7法测定水中化学需氧量时,用试亚铁灵作指示剂;用K2Cr2O7法测定水中Fe2+ 时,用二苯胺磺酸钠或试亚铁灵作指示剂。
K2Cr2O7是一强氧化剂。在酸性溶液中,K2Cr2O7与还原性物质作用时,Cr2O72-获得6mol电子被还原为Cr3+,反应式为:
Cr2O72- + 14H+ + 6e=2Cr3+ +7H2O
重铬酸钾的氧化能力(Cr2o72-/Cr3+=1.33V)小于KMnO4,但是重铬酸钾的稳定性大于高锰酸钾,且高锰酸钾溶液易自身分解为二氧化锰,而MnO2/Mn2+电对φMnO2/Mn2+=1.23<φCr2O72-/Cr3+=1.33V,这可能是测定水中有机物时K2Cr2O7法的氧化率大于KMnO4的原因之一。
8.1.1.2 化学需氧量的测定原理
化学需氧量是水体中存在有机物污染综合指标之一。在一定条件下,水中能被重铬酸钾氧化的有机物质的总量,以mgO2/L表示。
水样在强酸性条件下,过量的K2CrO7标准溶液与水中有机物等还原性物质反应后,以试亚铁灵为指标剂,用硫酸亚铁铵标准溶液回滴剩余的K2Cr2O7,计量点时,溶液由浅蓝色变为红色指示滴定终点,根据标准溶液的用量求出化学需氧量(COD,mgO2/L)。反应式如下:令C表示水中有机物等还原性物质。
2Cr2O72-+3C+16H+=4Cr3++3CO2+7H2O
(过量)(有机物)
Fe2++Cr2O72-+14H+=Fe3++2Cr3++7H2O
(剩余)
计量点时Fe(C12H8N2)33+Fe(C12H8N2)32+
(蓝色)(红色)
由于K2Cr2O7溶液呈橙色黄,还原产物Cr3+呈绿色,所以用(NH4)2Fe(SO4)2反滴定过程中,溶液的颜色变化是逐渐由橙黄色→蓝绿色→蓝色,滴定终点时立即由蓝色变为红色。
同时取无有机物蒸馏水做空白试验。
计算
式中——空白试验消耗(NH4)2Fe(SO4)2标准溶液的量,mL;
—— 滴定水样时消耗(NH4)2Fe(SO4)2标准溶液的量,mL;
C—— 硫酸亚铁铵标准溶液的浓度(NH4)2Fe(SO4)2,mg/L;
8—— 氧的摩尔质量 (1/2O2),g/mol;
——水样的量,mL.
应该指出,在滴定过程中所用K2CrO7标准溶液的浓度是1/6K2Cr2O7(mol/L)。
 爱华网
爱华网