| 药品编码 | 商品名 | 生产企业 | 剂型 | 规格 | 质量层次 | 医保编码 | 加入 |
|---|---|---|---|---|---|---|---|
| 26463 | 博璞青 | 天津红日药业股份有限公司 | 注射液 | 4000IU0.4ml*1 | GMP | 810 | 加入 |
| 26466 | 博璞青 | 天津红日药业股份有限公司 | 注射液 | 6000IU0.6ml*1 | GMP | 810 | 加入 |
| 57295 | 低分子肝素钙 | 河北常山生化药业有限公司 | 注射液(预充式) | 2050IU0.2ml*1 | GMP | 810 | 加入 |
| 38869 | 低分子肝素钙 | 赛诺菲安万特(杭州)制药有限公司 | 注射液 | 300ug0.4ml*2 | 专利或优质 | 810 | 加入 |
| 13297 | 低分子肝素钙 | 杭州九源基因工程有限公司 | 注射液 | 5000IU0.5ml*1 | GMP | 810 | 加入 |
| 13323 | 低分子肝素钙 | 法国赛诺菲温莎公司 | 注射液 | 300ug0.4ml*1 | GMP | 加入 | |
| 13327 | 低分子肝素钙 | 法国赛诺菲温莎公司 | 注射液 | 200ug0.3ml*1 | GMP | 加入 | |
| 62247 | 低分子肝素钙 | 深圳赛保尔生物药业有限公司 | 注射液 | 5000IU1ml*1 | GMP | 810 | 加入 |
| 36397 | 低分子肝素钙(预灌针) | 广东天普生化医药股份有限公司 | 注射液(预充式) | 6150IU0.6ml*1 | GMP | 810 | 加入 |
| 56427 | 低分子肝素钙注射液 | 河北常山生化药业有限公司 | 注射液(预充式) | 4100IU0.4ml*1 | GMP | 810 | 加入 |
| 36394 | 低分子肝素钙 | 广东天普生化医药股份有限公司 | 注射液 | 5000IU0.5ml*1 | GMP | 810 | 加入 |
| 13306 | 低分子量肝素钙 | 广东天普生化医药股份有限公司 | 注射液 | 2500IU0.5ml*1 | GMP | 810 | 加入 |
| 13300 | 低分子量肝素钙(预灌针) | 广东天普生化医药股份有限公司 | 注射液(预充式) | 4100IU0.4ml*1 | GMP | 810 | 加入 |
| 32746 | 立迈青 | 兆科药业(合肥)有限公司 | 冻干粉针 | 5000IU*1 | GMP | 810 | 加入 |
| 8218 | 立迈青 | 兆科药业(合肥)有限公司 | 冻干粉针 | 2500IU*1 | GMP | 加入 |
| 药品编码 | 商品名 | 生产企业 | 剂型 | 规格 | 质量层次 | 医保编码 | 加入 |
|---|---|---|---|---|---|---|---|
| 59763 | 赛博利 | 深圳赛保尔生物药业有限公司 | 注射液 | 5000IU0.5ml*1 | GMP | 810 | 加入 |
| 13275 | 速碧林 | 葛兰素史克(天津)有限公司 | 注射液(预充式) | 3075IU0.3ml*2 | 专利或优质 | 810 | 加入 |
| 13294 | 速碧林 | 葛兰素史克(天津)有限公司 | 注射液(预充式) | 6150IU0.6ml*2 | 专利或优质 | 810 | 加入 |
| 22555 | 速碧林 | 葛兰素史克(天津)有限公司 | 注射液(预充式) | 4100IU0.4ml*2 | 专利或优质 | 810 | 加入 |
| 28720 | 速碧林 | 葛兰素史克(天津)有限公司 | 注射液(预充式) | 4100IU0.4ml*1 | 专利或优质 | 810 | 加入 |
| 24099 | 尤尼舒 | 海南通用同盟药业有限公司 | 注射液 | 5000IU1ml*1 | GMP | 810 | 加入 |
兆科药业:港股00950李氏大药厂旗下公司
常山生化:
公司是国内6家获得低分子肝素钙注射剂批文厂家之一,其产品万脉舒享受发改委独家定价,市场占有率快速增长,份额已超过12%,本土企业第一。上市后,公司计划投资2000万支低分子肝素钙注射液项目。目前,公司的低分子肝素钙注射液在国内份额第一。
在低分子肝素钙注射剂方面,公司以流通环节管理政策颁布为导向,减少流通环节,调整产品价格策略,销售收入大幅增长。 毛利率比上年同期增减幅度较大的原因说明 公司主要产品之一低分子肝素钙注射液的毛利率较上年同期增长35.97%,主要是因为:低分子肝素钙注射液上游材料肝素钠原料药价格走低,导致直接材料低分子肝素钙原料药价格下降,另外公司改变低分子钙素钙注射液的运营模式,销售价格上升致使毛利率增长较快。
公司为肝素产业链一体化企业,优势特征明显,其中低分子肝素钙注射剂为单独定价品种,价格较同类产品高近一倍,产品质量亦优于国内同类产品,与国外产品标准相同。
公司低分子肝素钙注射剂市场份额在国内企业中位居首位,在整个低分子肝素产品中仅次于葛兰素史克的速碧林。目前公司低分子肝素的原料仍未获得批准,预计未来获批后可进行原料药替代,毛利率进一步提高。
2012Q1
单位:元 分行业或 营业收入 营业成本 毛利率(%) 分产品 分行业 生物医药制造业 243,127,281.16 123,356,489.2648.9% 分产品 肝素钠(注射级) 110,866,242.75 87,855,907.9620.79% 低分子肝素钙注射液117,175,279.71 24,141,293.70 79.4% 肝素钠注射液 776,502.52 429,020.00 44.75% 肝素钠(非注射级) 7,852,705.91 6,354,919.94 19.07% 其他 6,456,550.27 4,575,347.66 29.14% 接上表: 分行业或 营业收入 营业成本 毛利率比 分产品 比上年同 比上年同上年同期 期增减 期增减 增减(%) (%) (%) 分行业 生物医药制造业 -3.94% -26.99% 17.02% 分产品 肝素钠(注射级) -37.13%-27.32% -10.69% 低分子肝素钙注射液 237.61% 22.95% 35.97% 肝素钠注射液 243.3% 168.3% 15.45% 肝素钠(非注射级) -72.89% -70.4% -6.81% 其他 -16.54% -32.79%17.13%
2011年
肝素钠(注射级)(产品) | 28290.37| -23.16|36818.85| 102.56||低分子肝素钙注射液(产品)| 8693.32| 68.44| 5161.17| 72.35||肝素钠注射液(产品) | 22.62| -70.71| 77.22| -75.44||肝素钠(非注射级)(产品)| 3888.13| 4.67| 3714.63| 123.25||其他(产品) | 1430.29| 62.08| 882.45| -5.93||合计(产品) | 42347.93| -9.26|46671.80| 83.93|
分类产品 营业收入 营业成本 毛利率(%) 肝素钠(注射级) 28,290.3719,771.92 30.11% 低分子肝素钙注射液 8,693.324,436.90 48.96% 肝素钠注射液 22.62 15.99 29.31% 肝素钠(非注射级) 3,888.132,844.26 26.85% 其他 1,430.29 1,148.81 19.68% 合计 42,324.73 28,217.89 33.33%
红日药业的低分子肝素钙注射液半年收入2700万,同比增长40%,毛利率40%多一点,对比常山药业的低分子肝素钙半年收入1亿多,同比增长200%多,毛利率接近80%。所以,红日药业相比常山药业不是一个数量级的对手。
红日药业
2012H1
单位:元 分行业或分产品 营业收入 营业成本 毛利率(%) 分行业 成品药 246,946,865.43 44,958,203.88 81.79% 中药配方颗粒及 210,128,898.5860,867,395.87 71.03% 饮片 医疗器械 4,890,452.52 1,965,674 59.81% 分产品 血必净注射液 155,492,872.57 22,253,575 85.69% 盐酸法舒地尔注 63,512,258.446,315,511.65 90.06% 射液 低分子量肝素钙 27,593,394.5215,941,969.54 42.23% 注射液 中药配方颗粒 198,679,304.98 50,695,607.55 74.48% 中药饮片 11,449,593.6 10,171,788.32 11.16% 医疗器械 4,890,452.52 1,965,674 59.81% 其他产品 348,339.9 447,147.69 -28.37% 接上表: 营业收入比上 营业成本比上 毛利率比上 分行业或分产品 年同期增减(%)年同期增减(%) 年同期增减(%) 分行业 成品药 140.19% 62.38% 8.72% 中药配方颗粒及 76.9% 36.49% 8.57% 饮片 医疗器械 115.27% 102.17% 2.6% 分产品 血必净注射液 207.64% 134.28% 4.48% 盐酸法舒地尔注 95.67% 80.4% 0.84% 射液 低分子量肝素钙 39.3% 8.54% 16.37% 注射液 中药配方颗粒 83.91% 45.78% 6.67% 中药饮片 10.67% 9.98% 0.56% 医疗器械 115.27% 102.17% 2.6% 其他产品 -14.86% -21.39% 10.66%
受理号码 药品名称 药品类型 申请类型 注册分类 承办日期 企业名称 办理状态 状态开始时间 药品批准文号CYHB1105664 低分子量肝素钙注射液 化药 补充申请 2011-07-19 河北常山生化药业股份有限公司制证完毕-已发批件 2012-03-01 ----CYHB1105665 低分子量肝素钙注射液 化药 补充申请 2011-07-19 河北常山生化药业股份有限公司在审批 0000-00-00 ----CYHS1100496 那屈肝素钙注射液 化药 仿制 6 2011-07-14 河北常山生化药业股份有限公司 在审评2011-07-13CYHS1100495 那屈肝素钙注射液 化药 仿制 6 2011-07-14 河北常山生化药业股份有限公司 在审评2011-07-13CXHS1100079 那屈肝素钙 化药 新药 3.1 2011-07-12 河北常山生化药业股份有限公司 在审评2011-07-11CYHB0702091 吡拉西坦胶囊 化药 补充申请 2008-02-21 河北常山生化药业有限公司 制证完毕-已发批件2008-08-19 ----CYHS0604023 低分子量肝素钙 化药 已有国家标准 6 2006-08-02 河北常山生化药业股份有限公司在审评 2006-07-20CYHS0604024 低分子量肝素钠 化药 已有国家标准 6 2006-08-02 河北常山生化药业股份有限公司在审评 2006-07-20CYHS0601121 甲磺酸二氢麦角碱注射液 化药 已有国家标准 6 2006-05-24 河北常山生化药业股份有限公司制证完毕-已发批件 2008-10-16 ----CYHS0601120 甲磺酸二氢麦角碱注射液 化药 已有国家标准 6 2006-05-24 河北常山生化药业股份有限公司制证完毕-已发批件 2008-10-16 ----CYHS0600165 低分子量肝素钠注射液 化药 已有国家标准 6 2006-03-06河北常山生化药业股份有限公司 在审评 2006-03-03CYHS0506515 甲磺酸培氟沙星注射液 化药 已有国家标准 6 2005-11-04 河北常山生化药业股份有限公司制证完毕-已发批件 2006-09-06 国药准字H20066489CYHS0506514 甲磺酸培氟沙星注射液 化药 已有国家标准 6 2005-11-03 河北常山生化药业股份有限公司制证完毕-已发批件 2006-09-06 国药准字H20066488CYHS0504821 低分子量肝素钙注射液 化药 已有国家标准 6 2005-07-10河北常山生化药业股份有限公司 已发件 2006-04-04 国药准字H20063909CYHS0504822 低分子量肝素钙注射液 化药 已有国家标准 6 2005-07-10河北常山生化药业股份有限公司 已发件 2006-04-04 国药准字H20063910CYHS0501116 葛根素注射液 化药 已有国家标准 6 2005-03-13 河北常山生化药业股份有限公司 已发批件2005-09-23 国药准字H20057463CYHS0501117 葛根素注射液 化药 已有国家标准 6 2005-03-13 河北常山生化药业股份有限公司 已发批件2005-09-23 国药准字H20057464CYHS0501115 克林霉素磷酸酯注射液 化药 已有国家标准 6 2005-03-13 河北常山生化药业股份有限公司已发批件 2005-10-09 国药准字H20057537Y0402959 肝素钠注射液 化药 已有国家标准 6 2004-04-28 河北常山生化药业股份有限公司制证完毕-已发批件 2004-11-16 国药准字H20045512
(东诚生化:2009年公司本部已投资建设低分子肝素原料药生产线,子公司北方制药低分子肝素制剂生产线正在建设中,相关生产车间已完成装修改造。)CYHS1101527 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CYHS1101525 依诺肝素钠 化药 仿制 6 2012-08-01 烟台东诚生化股份有限公司 在审评2012-07-30CYHS1101526 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CYHS1101528 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CYHB1108427 依诺肝素钠 化药 补充申请 2012-03-31 杭州九源基因工程有限公司 在审评2012-03-29JYHB1101087 依诺肝素钠注射液 化药 补充申请 2011-11-25 无 在审评 2011-11-24JYHB1101083 依诺肝素钠注射液 化药 补充申请 2011-11-25 无 在审评 2011-11-24JYHB1101084 依诺肝素钠注射液 化药 补充申请 2011-11-25 无 在审评 2011-11-24JYHB1101086 依诺肝素钠注射液 化药 补充申请 2011-11-25 无 在审评 2011-11-24JYHB1101085 依诺肝素钠注射液 化药 补充申请 2011-11-25 无 在审评 2011-11-24CYHS1000822 依诺肝素钠 化药 仿制 6 2011-05-10 东营天东生化工业有限公司 在审评2011-05-09JYHB0901092 依诺肝素钠注射液 化药 补充申请 2010-01-21 无 制证完毕-已发批件 2012-05-15----JYHB0901093 依诺肝素钠注射液 化药 补充申请 2010-01-21 无 制证完毕-已发批件 2012-05-15----JYHB0901090 依诺肝素钠注射液 化药 补充申请 2010-01-21 无 制证完毕-已发批件 2012-05-15----JYHB0901094 依诺肝素钠注射液 化药 补充申请 2010-01-21 无 制证完毕-已发批件 2012-05-15----JYHB0901091 依诺肝素钠注射液 化药 补充申请 2010-01-21 无 制证完毕-已发批件 2012-05-15----JYHB0900523 依诺肝素钠注射液 化药 补充申请 2009-07-03 无 制证完毕-已发批件 2012-05-15----JYHB0900524 依诺肝素钠注射液 化药 补充申请 2009-07-03 无 制证完毕-已发批件 2012-05-15----JYHB0900522 依诺肝素钠注射液 化药 补充申请 2009-07-03 无 制证完毕-已发批件 2012-05-15----JYHB0900521 依诺肝素钠注射液 化药 补充申请 2009-07-03 无 制证完毕-已发批件 2012-05-15--
JYHB0900520 依诺肝素钠注射液 化药 补充申请 2009-07-03 无 制证完毕-已发批件 2012-05-15----CYHB0901935 依诺肝素钠注射液 化药 补充申请 2009-06-01 杭州九源基因工程有限公司 在审评2009-05-31CYHB0901934 依诺肝素钠注射液 化药 补充申请 2009-06-01 杭州九源基因工程有限公司 在审评2009-05-31CYHB0804915 依诺肝素钠注射液 化药 补充申请 2008-08-15 杭州九源基因工程有限公司 制证完毕-已发批件2009-04-21 ----CYHB0804916 依诺肝素钠注射液 化药 补充申请 2008-08-15 杭州九源基因工程有限公司 制证完毕-已发批件2009-04-21 ----JYHB0800099 依诺肝素钠注射液 化药 补充申请 2008-03-12 Sanofi-aventis France制证完毕-已发批件 2009-04-09 ----CYHS0700503 依诺肝素钠 化药 已有国家标准 6 2007-09-21 常州千红生化制药有限公司 在审评2007-09-19CYHS0700504 依诺肝素钠注射液 化药 已有国家标准 6 2007-09-20 常州千红生化制药有限公司在审评 2007-09-19CXHS0600723 注射用依诺肝素钠 化药 新药 5 2006-05-29 成都百裕科技制药有限公司 在审评2006-05-26CYHS0602514 依诺肝素钠注射液 化药 已有国家标准 6 2006-05-24 沈阳光大制药有限公司 已发通知件2008-04-09 ----CXHS0600205 依诺肝素钠 化药 新药 3.1 2006-04-26 海南长安国际制药有限公司制证完毕-已发批件 2008-06-20 ----CXHS0600439 注射用依诺肝素钠 化药 新药 5 2006-04-10 北京双鹭立生医药科技有限公司 在审评2006-04-07CXHS0600438 注射用依诺肝素钠 化药 新药 5 2006-04-10 北京双鹭立生医药科技有限公司 在审评2006-04-07CYHS0601205 依诺肝素钠注射液 化药 已有国家标准 6 2006-04-10 北京双鹭药业股份有限公司 在审评2006-04-07CYHS0601204 依诺肝素钠注射液 化药 已有国家标准 6 2006-04-10 北京双鹭药业股份有限公司 在审评2006-04-07CXHS0600437 依诺肝素钠 化药 新药 3.1 2006-04-10 北京双鹭药业股份有限公司 在审评2006-04-07CXHS0600224 依诺肝素钠 化药 新药 3.1 2006-04-02 南京臣功制药有限公司 制证完毕-已发批件2011-05-11 ----CYHS0600625 依诺肝素钠注射液 化药 已有国家标准 6 2006-04-02 南京臣功制药有限公司制证完毕-已发批件 2011-05-17 ----CYHS0600766 依诺肝素钠注射液 化药 已有国家标准 6 2006-03-21 南京健友药业有限公司 在审评2006-03-17CYHS0600732 依诺肝素钠注射液 化药 已有国家标准 6 2006-03-17 成都百裕科技制药有限公司 在审评2006-03-15
CXHS0600271 依诺肝素钠 化药 新药 3.1 2006-03-17 成都百裕科技制药有限公司 在审评2006-03-15CYHS0600624 依诺肝素钠注射液 化药 已有国家标准 6 2006-03-02 江苏江山制药有限公司 在审评2006-03-01CXHS0600223 依诺肝素钠 化药 新药 3.1 2006-03-02 江苏江山制药有限公司 在审评2006-03-01CXHS0503368 注射用依诺肝素钠 化药 新药 5 2006-03-01 苏州二叶制药有限公司 在审评2006-02-27CYHS0509683 依诺肝素钠注射液 化药 已有国家标准 6类 2006-02-24 苏州二叶制药有限公司 已发通知件2007-08-02 ----CYHS0509682 依诺肝素钠 化药 已有国家标准 6 2006-02-24 苏州二叶制药有限公司 在审批2009-01-22CXHS0503220 依诺肝素钠 化药 新药 3.1 2006-02-13 东营天东生化工业有限公司制证完毕-已发批件 2010-10-11 ----CYHS0509246 依诺肝素钠注射液 化药 已有国家标准 6 2006-02-13 山东潍坊制药厂有限公司制证完毕-已发批件 2010-10-11 ----CYHS0508375 依诺肝素钠 化药 已有国家标准 6 2006-01-04 南京健友生物化学制药有限公司 在审评2005-12-31CYHS0502969 依诺肝素钠注射液 化药 已有国家标准 6 2005-06-20 杭州九源基因工程有限公司已发件 2006-04-04 国药准字H20064067CYHS0502968 依诺肝素钠注射液 化药 已有国家标准 6 2005-06-20 杭州九源基因工程有限公司已发件 2006-04-04 国药准字H20064066CXHS0501101 依诺肝素钠 化药 新药 3.1 2005-06-16 杭州九源基因工程有限公司 已发件2006-04-19 国药准字H20060347
CYHS1101525 依诺肝素钠 化药 仿制 6 2012-08-01 烟台东诚生化股份有限公司 在审评2012-07-30CYHB1001163 低分子量肝素钠 化药 补充申请 2010-03-31 烟台东诚生化股份有限公司 制证完毕-已发批件2011-09-22 ----CYHB0901461 多西他赛 化药 补充申请 2009-03-24 烟台东诚生化股份有限公司 制证完毕-已发批件2009-06-25 ----CYHB0807916 肝素钠 化药 补充申请 2008-11-19 烟台东诚生化股份有限公司 在审评2008-11-18CYHS0700051 低分子量肝素钙 化药 已有国家标准 6 2007-05-25 烟台东诚生化有限公司 在审评2007-05-24CYHS0600428 维库溴铵 化药 已有国家标准 6 2006-06-02 烟台东诚生化有限公司 已发通知件2007-05-08 ----CYHS0600442 多西他赛 化药 已有国家标准 6 2006-04-10 烟台东诚生化有限公司 制证完毕-已发批件2008-03-05 国药准字H20083051CYHS0502061 卡络磺钠 化药 已有国家标准 6 2005-08-23 烟台东诚生化有限公司 制证完毕-已发批件2006-08-31 国药准字H20067438Y0400884 硫酸软骨素(供注射用) 化药 补充申请 2004-02-18 烟台东诚生化有限公司 制证完毕-已发批件2004-11-26 国药准字H20045882Y0305316 肝素钠 化药 补充申请 2003-12-12 烟台东诚生化有限公司 已发批件 2004-04-23----Y0305317 硫酸软骨素 化药 补充申请 2003-12-12 烟台东诚生化有限公司 已发批件 2004-05-14----FX20010165 硫酸软骨素 化药 已有国家标准 2001-07-19 烟台东诚生化有限公司 审批完毕0000-00-00
CYHS1101527 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CYHS1101526 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CYHS1101528 依诺肝素钠注射液 化药 仿制 6 2012-08-01 烟台北方制药有限公司 在审评2012-07-30CBHR1000024 注射用左卡尼汀 化药 复审 2010-08-10 烟台北方制药有限公司 制证完毕-已发批件2011-02-12 ----CYHB1006025 注射用甲硫氨酸维B1 化药 补充申请 2010-07-14 烟台北方制药有限公司 制证完毕-已发批件2011-01-05 ----CYHB1006024 注射用甲硫氨酸维B1 化药 补充申请 2010-07-14 烟台北方制药有限公司 制证完毕-已发批件2011-01-05 ----CYHB1001168 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB1001167 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB1001166 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB1001171 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB1001169 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB1001170 低分子量肝素钠注射液 化药 补充申请 2010-03-31 烟台北方制药有限公司 制证完毕-已发批件2011-09-22 ----CYHB0803074 注射用甲磺酸培氟沙星 化药 补充申请 2008-08-26 烟台北方制药有限公司 制证完毕-已发批件2009-04-08 ----CXHB0800229 注射用左卡尼汀 化药 补充申请 2008-05-19 烟台北方制药有限公司 制证完毕-已发批件2010-06-22 ----CYHS0700053 注射用低分子量肝素钙 化药 已有国家标准 6 2007-05-25 烟台北方制药有限公司 在审评2007-05-24CYHB0504227 硫酸软骨素注射液 化药 补充申请 2007-03-02 烟台北方制药有限公司 制证完毕-已发批件2008-10-29 ----CYHS0600574 注射用12种复合维生素 化药 已有国家标准 6 2006-06-27 烟台北方制药有限公司制证完毕-已发批件 2008-11-28 ----CYHS0600430 注射用维库溴铵 化药 已有国家标准 6 2006-06-02 烟台北方制药有限公司 已发通知件2007-04-13 ----CYHS0600429 注射用维库溴铵 化药 已有国家标准 6 2006-06-02 烟台北方制药有限公司 已发通知件2007-05-08 ----CYHS0600443 多西他赛注射液 化药 已有国家标准 6 2006-04-10 烟台北方制药有限公司制证完毕-已发批件 2008-11-12 ----
东诚生化1 200810013908.0 一种采用防腐剂生产鱼鳞胶原蛋白的方法2 200910229517.7 一种细胞色素C制备新方法3 201010623149.7 一种采用活性炭滤芯降低肝素钠400nm光吸收的生产工艺本发明公开了一种采用活性炭滤芯降低肝素钠400nm光吸收的新方法,多糖溶液经除杂、氧化后用活性炭滤芯过滤,能有效去除产品中含量较低的色素,降低产品的400nm光吸收。本发明提供了一种适用于肝素钠工业化大生产的控400nm光吸收方法,此方法简单安全,易于操作,不引入外来杂质,能有效降低产品的400nm光吸收。
4 201010623147.8 一种Ⅱ型胶原蛋白的提取方法5 201210095896.7 一种高效价肝素钠制备新工艺本发明公布了一种高效价肝素钠制备新工艺,属于生化原料药生产技术领域,尤其是涉及到高效价肝素钠的制备工艺。为提供收率高、成本低,质量好的肝素钠精品,开发出如下制备新工艺:以粗品肝素钠为原料,采用盐解、酶解工艺进行预处理,依次经离子絮凝、超滤、玻璃粉吸附三种除杂技术,可获得260nm光吸收极低的肝素钠中间体。再经简单氧化、采用改进后的溶剂进行分级,最终得到高效价的肝素钠精品。本发明具有提取条件温和、回收率高、成本低的特点,易于获得高效价、低杂质含量的肝素钠精品并适合于进行工业化大生产。
发明专利 (12 )条1 01803471.3 依诺肝素的新治疗应用阿文蒂斯药物股份有限公司本发明涉及依诺肝素在治疗脑缺血中的应用。
2 200610096955.7 依诺肝素及其制备方法江苏江山制药有限公司
3 200610051609.7 一种依诺肝素钠的纯化生产方法杭州九源基因工程有限公司本发明涉及一种依诺肝素钠的纯化生产方法,在水媒介中用长链季铵盐盐化肝素,经氯苄酯化后,在碱性条件下解聚得到分子量在3500-5500道尔顿之间的依诺肝素粗品,将上述解聚所得依诺肝素钠粗品经活性炭和大孔吸附树脂进行脱色后,得到能达到或优于欧洲药典4规定的颜色标准的依诺肝素成品,该方法经济实用,易于实现工业化生产,而且不会对依诺肝素钠的结构产生破 坏。
4 200680036711.8 依诺肝素在实施经皮冠状动脉介入治疗中的应用安万特医药股份有限公司
5 201010503282.9 一种依诺肝素的精制提纯方法山东郁茏生物科技有限公司
6 201010583647.3 一种依诺肝素钠的制备方法河北常山生化药业股份有限公司本发明公开了一种依诺肝素钠的制备方法,其步骤包括盐化、干燥、酯化、醇沉、氧化、醇沉、精滤、冻干制得成品。本发明采用亲水液相反应和疏水液相反应以及固相反应,将大分子肝素钠降解为具有特定结构的低分子肝素钠,并控制产物分子量和分子量分布范围,使导致出血危险的抗FIIa活性大幅降低,抗FXa活性相对提高,产品有效性和安全性优势明显,可有效预防静脉血栓栓塞症和肺栓塞症,可用于矫形外科、神经外科术前和术后血栓形成,可大大降低患中风风险,能更有效减少不稳定性冠状动脉综合症患者的死亡、心力衰竭、复发性心绞痛等,并可降低高甘油三脂血症,能有效解决普通未分级肝素及其衍生物长期使用后的出血、骨质疏松、诱导血小板减少等副作用
7 201110007946.7 一种提高依诺肝素钠注射液稳定性的生产工艺深圳市天道医药有限公司
8 201110241617.9 一种酶解-HPLC法检测依诺肝素的方法9 201210063865.3 一种依诺肝素钠酶解方法南京健友生化制药股份有限公司本发明公开了一种依诺肝素钠酶解方法,向依诺肝素钠溶液中加入乙酸钠/钙溶液和混合酶溶液,在温度为29~31℃下酶解66~72小时;其中所述乙酸钠/钙溶液的pH值为7,所述混合酶中各酶的酶活比例为肝素酶I∶肝素酶II∶肝素酶III=0.95~1.05∶1∶0.45~0.55。本方法得到的酶解产物通过HPLC检测,测得共有17组峰的峰面积面积大于总面积的0.3%,明显优于其他条件测得的结果。本发明提供的优化的酶解依诺肝素钠工艺,肝素酶III的用量明显减少,节约成本并且工艺简单、提高检测速度。
10 201210029323.4 一种依诺肝素钠及其生产纯化方法麦科罗夫(南通)生物制药有限公司本发明公开一种依诺肝素钠,依诺肝素钠的平均分子量在于3500-5500道尔顿之间,溶血栓生物活性100-125IU/mg,抗Xa与抗IIa的比值在3.3-5.3之间。依诺肝素钠生产纯化方法:肝素苄索氯铵盐的制备;肝素苄酯的制备:肝素苄酯的纯化;依诺肝素钠的制备;依诺肝素钠的纯化。依据本发明,并控制产品分子量和分布区间,最终得到的精品依诺肝素钠产品质量符合欧洲药典质量标准。本发明以肝素钠粗品为起始原料,能有效降低生产成本;精制肝素苄酯,稳定了最终产品质量,简化纯化难度,有效解决生产中色素问题,提高产品质量
11 201210064430.0 一种清真依诺肝素钠及其生产纯化方法麦科罗夫(南通)生物制药有限公司本发明公开了一种清真依诺肝素钠,清真依诺肝素钠的平均分子量在于3500-5500道尔顿之间,溶血栓生物活性100-125IU/mg,抗Xa与抗Ⅱa的比值在3.3-5.3之间;清真依诺肝素钠生产纯化方法,包括肝素钠粗品纯化,肝素钠盐化、干燥、酯化、醇沉降、碱降解、醇沉降、氧化、醇沉降、精滤、干燥制得成品。本发明以牛肺肝素钠粗品为起始原料,能有效降低生产成本;采用胰蛋白酶纯化肝素钠,操作方便、收率较高,所制的肝素钠精品具有质量稳定、纯度好、效价高等优点;精制肝素苄酯,稳定了最终产品质量,简化纯化难度,有效解决生产中色素问题,提高产品质量。
12 201210074424.3 一种由粗品肝素钠直接生产依诺肝素钠的方法
东营天东生化工业有限公司本发明涉及一种由粗品肝素钠直接生产依诺肝素钠的制备方法,其以粗品肝素钠为原料,通过有机溶剂分级沉淀除去粗品肝素钠中的大部分杂质,然后通过过氧化氢氧化除去部分残留的杂蛋白及色素等杂质,获得符合依诺肝素钠生产的高纯度的肝素钠,并以其为中间体,经肝素季铵盐制备、肝素苄酯的制备、对肝素苄酯进行碱解聚、以酸中和、醇沉淀,精制、脱色,脱水干燥,得到依诺肝素钠成品。本发明的方法大大减少了有机溶剂的使用,提高了生产效率,减少了对环境的影响,得到能达到或优于欧洲药典7.0版的依诺肝素钠成品,该方法操作简单,可实现工业化生产。
公司在研发领域将秉承“突破技术、引领行业”的理念,以自主创新为基础,继续首先以做大做强肝素系列产品为核心,积极开发低分子及超低分子肝素系列产品;其次,加强抗肿瘤药的研发和生产,主要是肝素的新型衍生物;再次,加强抗炎抗溃疡药物的生产和研发。
公司将逐步形成以肝素系列产品为核心,以抗肿瘤药物和抗炎抗溃疡药物为两翼的全新的战略发展布局。在公司募投项目投产后,公司将进一步扩大在肝素行业的竞争优势,在肝素制剂领域充分发挥自身独有的技术优势,保持肝素原料药及肝素制剂的协调发展。从更长远来看,公司除重点发展肝素系列产品外,将在抗肿瘤、抗炎抗溃疡药物领域积极投入,为公司未来在糖胺聚糖类药物领域的拓展奠定坚实的基础。(肝素是从动物小肠粘膜中提取的一种“葡糖胺聚糖”类物质,具有抗凝血、消炎、抗病毒、抗癌、调节血脂等作用。)
基于心脑血管用药市场、抗肿瘤药物市场和抗炎抗溃疡药物市场不断发展的趋势,公司将依托自身的技术、产品、定价及品牌优势等,以现有的肝素系列产品的深度拓展为基础,通过充分整合客户资源、供应商资源、人力资源、技术优势、品牌优势等各类优势资源,优化现有产品结构、加大研发投入和市场开发力度,逐步发展成为集研发、生产、销售于一身的大型糖类药物生产基地。为此,公司制订了未来两年的经营发展目标,具体如下:
(1)持续投入,做大做强肝素系列产品
公司的主导产品是肝素钠原料药、肝素钠制剂、低分子肝素钙制剂。公司将继续强化肝素系列产品的研发,不断改进生产工艺,进一步降低生产成本和提升产品质量及稳定性,形成更强的核心竞争优势。除巩固和发展国内市场外,公司还将实现肝素制剂产品对欧美发达国家的出口,逐步实现国产肝素制剂产品走向国际市场的目标。
(2)打造国内外一流的糖类药物研发中心
公司将以“突破技术、引领行业”的企业发展理念,继续引进高端生物制药专业人才,加大研发投入,加强多糖类药物自主创新及药品开发能力,用三年的时间把研发中心逐步打造成为拥有顶尖的技术人才、一流的软硬件研发设施、一流的研发理念的技术平台,为公司的长远发展打下坚实的基础。
多糖类药物在医药市场拥有广阔的发展空间。多糖类药物在抗肿瘤治疗和抗炎抗溃疡上具有独特的疗效,已成为近年来医药市场发展的热点之一。公司将借助自身的研发优势,重点开发多糖类抗肿瘤药物和抗炎抗溃疡药物,从而营造公司多糖类药物齐头并进的发展格局。
3月15日,河北常山生化药业股份有限公司承担的石家庄市重点科技项目“硫酸寡糖新型抗肿瘤药物的研究与开发”通过了鉴定验收,工艺技术达到国际先进水平。 经过近三年的研制开发,常山生化公司开发出质量高于现行的欧洲药典7.0版的硫酸寡糖新产品。该法制备的硫酸寡糖具有维持其高效活性的特定结构,其硫酸化程度高,具有较强的抗肿瘤活性,且毒副作用小。该工艺具备制备过程简单、生产周期短、成本低、产品收率高、质量稳定、制备过程中活性基团不受破坏等优点。
证券时报记者:公司新产品抗肿瘤、抗溃疡药目前有新的进展吗? 高树华:这两种药作为超低分子肝素,一旦研发出来,其市场规模将会超越所有的肝素和低分子肝素市场,价格会更高,利润率也会更高。但是短期内还不太现实,因为一种新药的研发需要一个比较复杂的过程和较长的时间周期。目前上述新药正在三期临床阶段,和国际保持同步。 证券时报记者:公司高端产品的发展有何突破? 高树华:肝素钠高端产品有不少突破,公司的那屈肝素产品,是国内唯一能和国外抗衡的,各项技术指标都不低于国外的产品,某些指标还要优于国外同类跨国公司的产品。比如依诺肝素,这是需求比较大的品种,我们有15项技术突破,都是独立开发。 证券时报记者:未来发展所面对的难题和困难有哪些? 高树华:主要是一些不可预测的困难,比如国家政策,如果除去这点,我们对自己是很有把握的。另外是市场大幅波动,尽管有注射制剂的支撑,但市场的快速波动对公司还是会有一定的影响,但影响不会太大。 证券时报记者:公司未来有什么发展重心? 高树华:未来公司发展的重心主要有两点,一是把低分子原料药做大做强,整个国际市场上低分子肝素原料药大概有15种,其中依诺肝素、那屈肝素、达替肝素,这三种低分子肝素在国际市场上需求量最大,我们要把这三种低分子肝素快速推向国际市场。由于做了低分子肝素原料药,第二个重点就是把这些原料药相对应的注射制剂也开发出来,发展的大思路就是原料为先头,制剂为目的,这样就保证不管原料药市场发生什么变化,公司整个经营状况不会受到太大影响。
与其他同行不同的是,常山药业出口业务额占总销售额的50%左右,出口依赖程度相对较低。
公司是国内6家获得低分子肝素钙注射剂批文厂家之一,其产品万脉舒享受发改委独家定价,市场占有率快速增长,份额已超过12%,本土企业第一。上市后,公司计划投资2000万支低分子肝素钙注射液项目。目前,公司的低分子肝素钙注射液在国内份额第一。同时,其生产的精制肝素原料药除了用于自行生产肝素钠注射液之外,还为国内多家标准肝素制剂生产企业提供精制肝素原料药,是国内最大的标准肝素制剂生产企业——天津生化的独家肝素原料药供应商。
在肝素粗品原料方面,有报告显示,常山药业的采购价格远远低于其他企业,比如2008年粗品平均采购价格比海普瑞低7.55%,比千红制药低13.63%;2009年,其采购价格比海普瑞低10.68%,比千红制药低9.26%。主要原因是其采购量小,灵活性较强。
上述扩产项目投产后,常山药业最需要解决的同样是肝素粗品来源。以往小规模的采购模式可能受到较大的限制,采购模式将向海普瑞等大企业靠拢,但公司与国内大型肝素粗品供应商的合作基础比较薄弱,未来资源竞争处于劣势。
不过,常山药业拟收购泰康药业74.18%股权,该公司主营肝素钠、低分子量肝素钙、低分子量肝素钠(达肝素钠、依诺肝素钠)等,该收购将有利于加快公司取得低分子肝素钙原料药批件。
1 201010583647.3 一种依诺肝素钠的制备方法本发明公开了一种依诺肝素钠的制备方法,其步骤包括盐化、干燥、酯化、醇沉、氧化、醇沉、精滤、冻干制得成品。本发明采用亲水液相反应和疏水液相反应以及固相反应,将大分子肝素钠降解为具有特定结构的低分子肝素钠,并控制产物分子量和分子量分布范围,使导致出血危险的抗FIIa活性大幅降低,抗FXa活性相对提高,产品有效性和安全性优势明显,可有效预防静脉血栓栓塞症和肺栓塞症,可用于矫形外科、神经外科术前和术后血栓形成,可大大降低患中风风险,能更有效减少不稳定性冠状动脉综合症患者的死亡、心力衰竭、复发性心绞痛等,并可降低高甘油三脂血症,能有效解决普通未分级肝素及其衍生物长期使用后的出血、骨质疏松、诱导血小板减少等副作用。
2 201110457982.3 一种达肝素钠制备工艺
本发明公开了一种达肝素钠制备工艺,包括制备肝素钠溶液、制备肝素降解液、制备还原液、制备粗品、精制、冻干等步骤。所得产品重均分子量为5500~6500,峰位分子量为3500~6000,分子量小于3000的组分不大于13%,分子量大于8000的组分不大于15%,抗Xa活性≥130IU/mg。原料来源丰富、产率高、质量稳定可靠、纯度高、成本低、工艺简单、操作方便,无三废排放。产品达肝素钠具有抗凝血、抗血栓、抗肿瘤、抗炎、抗过敏等作用和调节血脂的功效,疗效显著,可用于预防普通外科、矫形外科、神经外科的术前和术后的血栓形成,可有效防止缺血性中风患者的静脉血栓栓塞症,可大大降低患中风风险,可有效防止血液体外循环引起的凝固,能有效防止不稳定性冠心病,使用范围广泛。
玻璃酸钠(又称透明质酸钠)是一种糖胺聚糖,在生物医药、生物材料、功能食品以及化妆品等领域的应用已获得广泛的认可。鉴于我国国家食品药品监督管理局对该产品依据用途所进行的行政管理:作为药品,用于骨关节腔注射治疗骨关节炎、干眼症和伤口愈合,称为玻璃酸钠;作为生物材料,用于眼科手术的填充剂、外科手术防止术后组织粘连的隔离剂以及医学整形美容领域中作为填充,称为透明质酸。2012年5月19日,在上海景峰制药有限公司主办的“玻璃酸钠研讨会暨《玻璃酸钠生产与临床应用》新书发布会”上,来自此领域专家聚集一堂,就玻璃酸钠在临床上的应用展开了细致的探讨。
玻璃酸钠广泛分布在动物和人体组织及细胞外基质中,在眼玻璃体、房水、滑液、皮肤和脐带中含量较高,被认为是一种填充空间、稳定结构、涂层细胞和保护细胞的多糖。
玻璃酸钠在骨科中的应用
——上海交通大学附属第六人民医院骨科、关节镜外科专家皇甫小桥教授
玻璃酸钠为关节滑液的主要成份,是软骨基质的成份之一。在关节腔内起润滑作用,减少组织之间的摩擦,同时发挥弹性作用,缓冲应力对关节软骨的作用,发挥应有的生理功能。骨性关节炎是骨科临床上的常见病,膝关节是最常累及的部位之一。由于膝关节是身体主要的负重关节,故膝关节骨性关节炎可导致患者较严重的功能障碍。通过实验及临床应用均证明玻璃酸钠是治疗骨性关节炎的一种安全、理想、有效的药物。具有参与细胞外液中电解质及水分调节、润滑关节、抗御感染、参与创伤愈合等多种生理功能,对关节的保护、营养及功能的发挥均起重要的作用,主要表现为关节腔的润滑、覆盖屏障及缓冲应力。
在各种致病原因作用下,关节腔滑膜成分改变,玻璃酸钠含量减少或关节功能减退,造成关节软骨腐蚀、破坏,产生疼痛、活动障碍。补充外源性的玻璃酸钠可以提高滑膜中玻璃酸钠的含量,重新形成自然屏障,防止软骨基质进一步破坏消失;改善病理状态下滑膜的生物学功能,减轻或消除关节磨擦及疼痛;通过其抑制白细胞移动及趋化作用,减少滑膜通透性、增加高分子玻璃酸钠生成,减少关节内渗液;覆盖和保护痛觉感觉器,与疼痛介质结合,缓解疼痛;与糖蛋白结合,阻止该物质参与炎症过程,同时玻璃酸钠进入软骨基质,与糖蛋白形成聚合体,修复损伤的软骨。所以玻璃酸钠对轻中度的膝关节骨性关节炎具有良好的疗效。
玻璃酸钠在眼科中的应用
——南方医科大学附属南方医院眼科专家汤明芳教授
在眼玻璃体中含有大量的玻璃酸钠,与胶原纤维、可溶性蛋白质共同构成玻璃体。Hedbys等发现,角膜对水的作用是由基质中玻璃酸钠网状结构所产生。1%~3%玻璃酸钠用作眼科手术理想黏弹剂已有三十多年的历史。在手术中可以有效支撑前房;提供清晰的手术视野;并且易于自注射针头推出,术后易于冲洗;涂布于眼内组织表面及手术器械表面形成保护膜,使角膜和小梁内皮细胞、晶状体、睫状体上皮细胞等避免机械性损伤;避免角膜等组织在手术过程中暴露于空气所致的干燥;并可加速角膜损伤的愈合。
玻璃酸钠具有显著的亲水能力和润滑作用,因此,可明显缓解眼干燥症的疼痛、痒、烧灼感、异物感等临床症状,明显延长泪膜破裂时间。研究者一致认为,玻璃酸钠可能与角膜表面和泪膜发生作用,对泪膜起稳定作用,从而可对眼部产生湿润和润滑作用,消除眼部的不适症状。玻璃酸钠除了作为主要成分配制成滴眼液治疗干眼症以外,还作为眼部给药传输系统的媒介而广泛地应用于眼用制剂中。
玻璃酸钠在医学美容中的应用
——上海交通大学医学院附属第九人民医院皮肤科专家徐慧教授
如今的美容整形已经不仅仅是为了修复残缺,而更多是为了追求"完美",精致的五官,顺滑细腻的肌肤和时尚的妆容。玻璃酸钠藉其独特的生物活性作为注射用软组织填充剂,用于注射到皮肤或皮下组织内使皮肤凹陷、缺损得以填充,达到纠正缺陷,恢复完美皮肤外观。
注射美容是临床非手术整形美容的一种,之所以能在当今盛行,主要因为它的确有着很多优点。并且随着科技的发展,填充材料的品种日益丰富,更具安全性和可控性。首先,注射填充有着许多手术植入假体材料的不可替代性,尤其是其对细小轮廓的修整所体现的自然美感胜于手术治疗;其次,微创微痛和基本无需停工符合现代快节奏的生活步伐。
玻璃酸钠在伤口修复中的应用
——第二军医大学长海医院药学部专家王忠壮教授
玻璃酸钠主要由成纤维细胞合成,分布于皮肤真皮和表皮的颗粒层及棘层,是体内唯一不含硫酸基团并能以游离形式存在或与蛋白质以共价结合而起作用的一种糖胺聚糖。皮肤中的玻璃酸钠可与其它糖胺聚糖和胶原等形成富含水的凝胶,是细胞代谢过程中营养物质的供给和废物排泄的介质。玻璃酸钠通过与细胞膜上的受体结合,引导一系列生理生化反应,促进细胞的分化和移动,对皮肤创伤的修复和再生具有重要作用。玻璃酸钠可加快受伤动物上皮细胞的迁移速度,促进伤口愈合所必需的巨噬细胞的调集。此外,玻璃酸钠还传运某些蛋白质和多肽如生长因子等至创伤部位,而这些因子对创伤的愈合起重要的作用。
迄今为止,国家食品药品监督管理局没有正式批准玻璃酸钠用于皮肤伤口修复,部分临床医生和研究小组进行了一些这方面的有益尝试,取得满意效果,证明有益于伤口的愈合和减少瘢痕生成,对于新药、新适应症开发有启示。国外已经有作为药品的伤口治疗用玻璃酸钠制剂用于临床。
《玻璃酸钠生产与临床应用》主编顾其胜教授
《玻璃酸钠生产与临床应用》是由该行业中资深专家顾其胜教授等十多位专家及奋战在一线经验丰富的年轻学者和专业人员,根据其本人的工作性质和多年的研究以及常年积累的工作经验,以实用为准则、以临床为重点,历时两年编写而成。该书主要包括概述、制备工艺、产品标准与质控、产品衍生物、在眼科中的应用、在骨科中的应用、在腹盆腔外科中的应用、在医学美容中的应用、在伤口修复中的应用等内容。每一章都首先阐述基本概念与最新理论,然后全面总结玻璃酸钠在该方面的实践经验,最后在理论与实践相结合的基础上,归纳、提炼而成。读者可以通过阅读本书,既能熟悉并掌握玻璃酸钠制备与检验、规模化生产出合格产品,又能按其临床病症知道如何使用该产品。既能了解、熟悉并掌握玻璃酸钠相关知识,又能了解该物质的发展趋势和最新动态,可以较为全面地深切认识玻璃酸钠。
透明质酸的医疗用途的不断扩大,拥有广阔的市场前景。我国国内企业用发酵法生产透明质酸始于上世纪80年代末至90年代初,截止2011年9月25日,国家食品药品监督管理局网站上可查阅的产品及其适应症的信息:药品一栏国产药品关键字玻璃酸钠共有23条记录,包含4种原料,2中药用辅料,7种滴眼液和10种注射液;医疗器械一栏医疗器械关键字玻璃酸钠共有74条记录。
2012H1 应收不多,但是存货暴增,导致经营现金流为负。经分析,主要是原材料存货比较多。
2012年开年,作为肝素钠原料的肝素钠粗品价格开始快速反弹,一度从去年年底的15000元/亿单位反弹至上周的23000元/亿单位,上涨幅度超过50%,离去年的高点26000元/亿单位仅一步之遥。相关分析人士认为,今年肝素钠粗品价格创新高的可能性较大。
肝素钠粗品的价格上涨,对于以其为主要原料的肝素钠原料药厂家来说,是件喜忧参半的事,一方面成本的上涨挤压着产品利润,另一方面成本推动产品价格的上涨也将对整个肝素钠市场有所促进,反而会对相关公司经营业绩以及行业发展有一定好处。不过,业内对肝素钠原料药提价,是否能成功转移成本有所疑虑。此前肝素钠粗品的上涨,一定程度上是因为肝素钠原料药价格所带动,而本轮上涨则由于今年生猪出栏率不高,猪肉价格上涨。目前国内市场上,猪小肠、肠衣等原材料处于供不应求状况,因此,相关企业都在市场抢购原材料。在已上市的肝素钠企业中,海普瑞、千红制药、常山药业的肝素钠粗品都需要大量采购,若肝素钠粗品价格持续上涨,下游原料药无法及时提价,或对相关公司有所影响。
常山药业是我国在肝素行业中唯一拥有完整产业链的公司,产品从粗品肝素、肝素的中间体、肝素的原料药、到肝素注射剂、再到低分子肝素原料药,最后到产品的终端低分子肝素注射剂。
姬胜利介绍,如果光生产注射制剂,而不生产原料药,由于国家对肝素注射制剂产品实施最高零售价限制,那么当肝素类原料药供不应求,价格持续上涨的情况下,成本不可控,导致企业面临巨大的成本压力。如果只生产原料药,不生产制剂,受国际市场波动、产品专利到期以及低价格仿制药出现的影响,原料药价格会持续走低,对业绩产生巨大影响。
常山药业和同行业相比,既有上游产品肝素和低分子肝素原料药,也有下游产品肝素和低分子肝素注射制剂,大大提升了抗风险能力。因为在原料药下跌的同时,注射制剂的成本也会跟随下跌,制剂市场售价由发改委直接定价,这就使注射制剂的利润增加。2012年第一季度,公司在低分子肝素钙注射制剂毛利的增长率更是达到了惊人的471%。
近两年常山药业注射制剂的销量一直保持稳定增长,公司预计2012年将占全部产品销量的40%。
近两年我几乎每个月都要到国外的客户那里去给他们讲课。”总经理姬胜利说。
在将产品推向国际市场时,常山药业发现有很多潜在客户以电话或邮件的方式咨询产品情况。虽然他们表示了极大兴趣,但是对产品的性能特点和质量控制都不熟悉。
对这种状况,公司管理层制定了教课式的营销方式,出国当面授课通过技术指导让客户对产品深入了解。同时,讲课前双方签订意向协议,购买产品后公司实行长期的跟踪服务策略。该方式取得了良好的市场反应,由于产能的限制,很多订单公司都无力去接,但这种技术指导的方式,对公司未来募投项目投产后,其产品的营销做了有力高效的前期铺垫。
我国的肝素原料药市场,多数用于出口。这意味着每获得一个国家的质量标准体系认证,就等于打开了一个新的市场。公司于2008年通过了欧洲药品质量管理局现场检查,取得肝素原料药CEP证书(欧洲药典适应性认证);2009年获得法国GMP证书(药品质量管理规范),由于欧盟的认证体系只要在一个国家获得GMP证书,在整个欧洲就可以销售,公司等于打开了欧洲市场。
上市后,公司成功收购常州泰康制药有限公司,其产品此前通过了日本药品医疗器械局的现场检查。此举进一步加强了公司实力,产品也成功进入日本市场。
目前,公司肝素原料药在欧洲、美国、印度、俄罗斯和乌克兰都已经注册成功;低分子肝素依诺肝素已在俄罗斯注册成功;肝素钠注射液和那屈肝素钙注射液在摩尔多瓦注册成功,其标志着公司产品可以在中美洲和南美洲市场进行销售。在世界各地积极推进原料药以及注射制剂的注册,是近几年公司重点推进的事情之一。
募投项目释放产能
上市公司募集资金使用情况,一直是投资者关注的问题。虽然常山药业在IPO招股说明书和年报中都做了相关披露,但对实际募投项目进展情况,投资者在参观前心里还是不太踏实。在随后走访募投项目基地时,一行人看到一栋栋建筑拔地而起。投资者一边实地考察项目进展情况,一边听相关负责人讲解。
据了解,常山药业募投项目拟建的新厂区占地面积约200亩,总投资约5亿元。项目建成后,预计将实现年生产肝素钠原料药3万亿单位,低分子量肝素原料药2000公斤,低分子量肝素注射液2000万支的生产能力。目前一期项目的办公楼、研发质检楼、生产车间(包括原料药、透明质酸年产20吨)、食堂和职工宿舍都已经建好,下一步将进行内部装修、设备装进。预计新厂区原料药今年年底建设完成,明年年初投产。
厂区由外国行业内知名公司设计完成,主要设备按照国际上最高标准进行招标引进,以应对国际上对肝素类药品检验标准的日趋严格。公司表示,生产车间建设完成后,将成为国内最好的生产肝素、低分子肝素原料药的车间。
国际一流的生产车间为常山药业已开发的多种新产品在未来的顺利投产奠定了基础。肝素系列新产品中,公司正在开发的有瑞肝素、贝米肝素、帕肝素钠、阿地肝素以及超低分子肝素,其中超低分子肝素是肝素系列产品的一代新产品,具有副作用更小、抗肿瘤等效果。公司的透明质酸经过科研人员多年的技术攻关,已取得较好的收率指标,并将成为公司新的业绩增长点。此外,公司还开发了新的生物药物包括抗肿瘤的长效靶向药物生物技术产品和硫酸皮肤素等。
“未来我们的肝素品种会更多、规模会更大。在肝素以外会涉足更多的品种,全公司人员将致力于把常山药业打造为国际一流的生物制药企业!”董事长高树华说。
常山药业(300255)有望从全球低分子肝素制剂最畅销药物"依诺肝素钠"中分得一杯羹。公司30日公告,其"一种依诺肝素钠的制备方法"收到国家知识产权局办法的发明专利证书。该专利是公司核心技术的延伸,应用该专利生产的依诺肝素钠原料药现处于新药申请生产的注册核准阶段,已有小批量产品对外出口。 依诺肝素钠由Sanofi-Aventis生产,属低分子肝素钠制剂中最畅销药物,目前以依诺肝素钠为代表的部分专利药品保护期陆续到期,市场垄断正被打破。山德士公司的依诺肝素钠仿制药最先通过美国FDA认证,山德士肝素钠注射液于2011年6月8日在美国上市,曾被认为将促进中国肝素钠原料药的出口,其中,千红制药因为直接为山德士提供符合FDA标准的注射级肝素钠原料药,股价随之高歌猛进。而常山药业凭借该专利,有望成为依诺肝素钠领域的又一重量级仿制药提供商。
总经理姬胜利:支撑肝素价格的因素主要是新产品,原来的各种低分子肝素专利陆续到期后,仿制药进入市场竞争,所以必须要降价。但并不是说未来价格会持续下跌,第一是因为这些产品的需求量全世界每年增长率9%~11%,中国每年增长率20%以上。第二以肝素为原料开发的新产品超低分子肝素,现在正在做三期临床,一旦临床试验完成,就将迅速推向市场,这些创新药推向市场后又会带动原料市场价格往上走,超低分子肝素与低分子肝素和普通分子肝素比较,还具有抗肿瘤作用,必定会带动其销量大增。
在公司的高管中,值得一提的是常山药业现任总经理姬胜利。 《每日经济新闻》记者了解后发现,曾经是山东大学副教授的常山药业总经理姬胜利,2008年加入常山药业,其2010年年薪高达74.4万元。这一收入不仅是常山药业所有高管中年薪最高的,而且数倍于公司其他高管的年薪,甚至高于同行业公司与行业龙头事实上,常山药业不仅给了姬胜利相当高的年薪,还在公司上市前夕,给了他“突击入股”的机会。2009年12月29日,常山药业进行了增资扩股,姬胜利以每股4元的价格认购367.50万股,总金额合计1470万元,增资完成后姬胜利持有常山药业的股份比例为4.55%。然而有意思的是,姬胜利“突击入股”所用的这笔钱绝大部分却是向别人借的。 北京市竞天公诚律师事务所为常山药业出具的一份《补充法律意见书》透露,姬胜利1470万元增资款中,70万元为姬胜利家庭自有资金;其余1400万元是借款,年利率为6%。但无论怎么算,姬胜利的这笔投资相当划算,以常山药业目前确定的28元/股的发行价计算,仅用了不到两年时间,这笔股权投资的市值就已经翻了7倍,逾1亿元,即使按照约定减去利息,姬胜利也仍然差不多可以跻身亿万富翁行列。
高树华先生于1993年开始从事肝素系列产品的研发生产至今,期间成功研制出无酸化蛋白质共沉淀技术、动态离子交换吸附技术、脱色树脂纯化工艺等专有技术,并取得了发明专利的“一种低分子量肝素钙的生产工艺”。为加强高端人才储备, 公司于2008年聘用国内糖生物学与糖工程专业的专家姬胜利博士为公司总经理。姬胜利博士曾参与多项糖类新产品的开发研究,承担过18项国家和省级科研课题,获得“肝素中硫酸皮肤素定量检测方法”“一种硫酸皮肤素、及其衍生物的口服剂和其制备防范”等国家发明专利,发表论文近70篇,主编或参编出版著作8部,并承担和参与完成3项国家自然科学基金项目,是行业权威专家。
公司独立提出低分子量肝素钙注射液的国家标准(“YBH03832006标准”),并经国家药监局审核通
董事长高树华诚恳、耐心回答问题的态度给投资者留下了深刻印象,高树华不仅是生物制药领域的高级工程师,年过花甲的他从1992年就从事肝素产品研究,是业内不折不扣的专家。董事长表示对于目前常山药业而言,规模虽小,但企业的抗风险能力却很强。常山药业 董事长高树华(虽然企业规模很小,但抗风险能力却很强,因为产品的产业链比较完整)近年来,随着肝素钠价格的不断下跌,行业中无论企业收入和利润均出现大幅下滑,作为龙头企业的海普瑞,去年年报显示公司营业收入下滑35%,利润总额更是下跌了近50%,常山药业药业去年总收入下滑9%,而利润总额却增长了18.55%,常山药业董事长高树华认为,这是因为公司肝素钠完整产业链化解了不利因素。常山药业 董事长高树华(同行业的企业收入下降主要是由于价格的下降,而常山药业不仅有原料药,还有注射剂)配音:年报显示,公司未来将以肝素系列产品为核心,以抗肿瘤药物和抗炎抗溃疡药物为两翼的全新的战略发展布局,对于目前公司在抗肿瘤方面的研究,高树华明确表示非常看好该领域在未来的成长空间。常山药业 董事长高树华(抗肿瘤药未来的空间将超过肝素类,目前和美国等欧美企业处以同一研发水平)在谈到与国内外同行业的竞争时,高树华表示尽管目前同行业竞争激烈,但公司从不以价格战作为竞争的手段,公司长期坚持在技术研发上下功夫。
透明质酸钠也叫玻璃酸钠。1934年,Meyer等自牛眼玻璃体(hyaloidbody)分离出一种含糖醛酸(uronic acid)和氨基己糖的高分子多糖,命名为“hyaluronicacid”。该词由“hyaloid”(透明的、玻璃状的)和“uronicacid”组合而成,《生物化学名词》译为“透明质酸”,《中国药典药》和国家药品标准称为“玻璃酸”。在生理中性环境中,hyaluronicacid是一个聚阴离子。1985年,Balazs等建议“hyaluronan”一词作为此种多糖的总称,不管其处于何种程度的解离度。“hyaluronan”已广泛应用,涵盖了任何状态的透明质酸及其盐(hyaluronate),通常将其译为“透明质酸”,缩写为HA。在目前,通常将药准字号的HA制品称作玻璃酸钠注射液,而械准字号HA制品称作医用透明质酸钠凝胶。
不同工艺生产的透明质酸的分子量也各不相同,天然性状的透明质酸钠的分子量一般在80万~250万之间,通常认为透明质酸钠的分子量越高则粘弹性越好,疗效也就越好
微生物发酵法制取: 用Streptococcuszooepidemics(兽疫链球菌)的突变体(mutant)发酵制取。此突变体无溶血活性,产透明质酸钠量大,产品分子量可达250万。从动物组织提取: 用蛋白酶去除蛋白质,以十六烷基氯化吡啶单离HA,以足量氯仿进一步去除蛋白质。纯品中氨基酸含量仅为0.35%,分子量最高可达120万。
眼科手术: 眼科手术辅助用医疗器械,用于白内障摘除术和人工晶体手术等。骨科手术: 骨科手术,主要用于预防肌腱粘连,缝合术后于暴露肌腱吻合处、腱周、腱间均匀涂抹本品,也可于损伤修复部鞘内或局部注射,或二者并行,视情况而定。关节腔内注射: 常用于治疗骨关节炎及类风湿性关节炎等。妇科手术: 可涂布于子宫肌瘤剥除术、剖腹产术以及输卵管复通术后的吻合口表面;宫腔镜下的输卵管通液后以及宫腔粘连分解术后软组织粗糙面涂布;或于子宫内膜异位症和肿瘤造成的盆腔粘连松解术后使用。各种腹腔镜手术: 在直视条件下,通过导管将本品涂布于组织粗糙面。其它手术: 如甲状腺手术、泌尿外科、耳科手术后防止炎性粘连反应等。
透明质酸的生产过程和技术决定了质量优劣的差异,所以在使用上一定要是正确来源生产的产品才能有治疗的功效.一般而言,提炼的方法有三种: 1、动物组织:主要原料是鸡冠和牛眼玻璃体等.用丙酮或乙醇将原料脱脂、脱水,用蒸馏水浸泡、过滤,然后以氯化钠水溶液和氯仿溶液处理,之后加入胰蛋白酶保温后得到混合液,最后用离子交换剂进行处理、纯化得到精制的透明质酸.这种方法提取率极低,仅1%左右,分离过程复杂,致使透明质酸价格昂贵,达5000美元/公斤,限制了在化妆品中大的量使用. 2、微生物发酵:以葡萄糖作为碳源发酵液.在培养基中发酵48小时,发酵结束后,过滤除去菌丝体和杂质,然后用醇沉淀法等简单操作即得到高纯度的产物.采用发酵法制造的透明质酸,优点是能按商品设计来设定分子量大小.发酵法的关键在于菌种的选择,目前多选用链球菌、乳酸球菌类等. 3、化学合成:采用天然酶聚合反应;首先使用多糖类聚合物合成“透明质酸氧氮杂环戊烯衍生物”,然后添加水分解酶,制造出衍生物和酶的复合体,最后在90度摄氏反应液中清除其中的酶,就合成了透明质酸.采用人工合成法可大大降低透明质酸的制造成本,但结构较不精纯. 同样是透明质酸的产品,因为原料来源及制成技术的差别,对效果有明显的影响.产品的浓度不能作为选择产品的参考,纯度、分子量、3D立体结构才会直接影响透明质酸的吸水效果.通常分子量愈大、网状结构愈完整,有最好的吸水效果.坊间保养品、化妆品盛行,但许多业者自制的透明质酸,便宜,可是不一定有效果.甚至有人推行的口服的透明质酸,经过肠胃吸收之后会分解成醣类及氨基酸的小单位分子,还是必须透过自体合成等复霒步骤才能生成在皮肤、结镳组织中,其效果也必须要打折扣.
商品名 生产厂家 制备工艺 分子量 包装规格 保存爱维 山东博士伦福瑞达 微生物发酵 150~250万 0.5ml,1ml 遮光,2~8℃其胜 上海其胜生物制剂 微生物发酵 平均200万 0.5ml,0.8ml 遮光,2~8℃施沛特 山东博士伦福瑞达 微生物发酵 150~250万 2.0ml:20mg 遮光,密闭施沛克 山东博士伦福瑞达 微生物发酵 150~250万 2.0ml,3.0ml 遮光,2~8℃益术康 常州药物研究所 动物组织提取 200万以上 2ml,2.5ml,3ml 遮光,2~8℃佰备 上海佰加壹制药 动物组织提取 80万以上 2.5ml:25mg 遮光,2~8℃阿尔治 日本生化学工业 动物组织提取 80~120万 2.5ml:25mg 25℃以下免冻
口服透明质酸被肌肤吸收后,会形成独特的三维立体结构,为真皮层胶原蛋白和弹性纤维的合成提供优越的外部环境,还可像海绵一样吸收数百倍体积的水分子,维持表皮结缔组织细胞间脂质的水份。由于此技术含量较高,且临床试验阶段较为漫长,目前只有日本的ESMAY拥有此项顶尖技术,当然,在此领域我国也不甘落后,上海的某研究所和江南大学等机构也已经获得一些质的进步,我们拭目以待。
国家食品药品监督管理局将克赛®通用名由“低分子肝素钠”更改为“依诺肝素钠”,这一名称的改变有何临床意义? 李玉珍教授:抗凝治疗的进展促进了心血管防治的发展,特别是低分子肝素的研发应用促使抗凝治疗进入到全新时代,与普通肝素相比,低分子肝素作为新一类抗凝药物具有更强的抗凝效能,对血小板功能影响少、副作用小、皮下注射吸收好、体内半衰期较长等诸多优点,在临床被广泛应用。 国内外应用于临床的低分子肝素有十余种,由于既往抗凝领域的一些学术概念未得到精确区分,普遍认为低分子肝素都是一样的。实际上,由于生产工艺、化学结构等的不同,不同的低分子肝素临床疗效和适应证也存在差异,因此,WHO、FDA等权威机构在几年前就明确指出:一种低分子肝素的特点不能随意推广到另一种低分子肝素上,针对某一特定的低分子肝素的临床研究的结果不能推广到其他的低分子肝素。同时美国FDA对此已经进行了分类管理,按照生产厂家及来源的不同将低分子肝素分为不同品种。此次,我国SFDA(国家食品药品监督管理局)将克赛®的通用名由“低分子肝素钠”更改为“依诺肝素钠”正是基于不同的低分子肝素临床疗效和适应征是不同的。尽管低分子肝素都是由普通肝素解聚而成,但不同的制造商采用了不同的化学或酶学解聚过程,依诺肝素钠是经苄基酯化后在碱性条件下解聚而得的,独特的生产工艺使得其化学结构(链的长度、链的序列、指纹图谱结构等)、化合物平均分子量、抗凝血酶Ⅲ和HCII的结合、抗Xa/抗IIa比等都具有独特性。由于独特的制造工艺决定了依诺肝素钠疗效特征和安全性的不可复制性,ACC/AHA指南对于唯一推荐的低分子肝素明确强调是依诺肝素,而不是泛指低分子肝素.;同时,这次更名也是为了与国际接轨,因为全球范围内均使用“依诺肝素钠”作为克赛的通用名。 毫无疑问,依诺肝素钠的更名有着重要的临床意义:促使临床工作者对于同类药物的认知更加精确化和个体化。 心血管网:那我们如何对抗凝药物进行综合评估,来帮助临床应用时更好的选择合适的药物呢? 李玉珍教授:在临床治疗工作中选择抗凝药物应该严格遵循药物适应证、循证证据和治疗指南。例如,目前用于临床的三种低分子肝素中,内科病人VTE预防和肺栓塞(PE)治疗只能选用克赛,其他两种药物没有这两个适应症。对药物理化性质和物理生化特性进行综合评价的同时,还要注重临床评价。临床评价药物的科学方法是高质量循证医学证据,而不是个体的病例,只有经过大量研究和临床实践证实有着可靠疗效和安全性的药物才能用于临床患者的治疗。我们可以看到,克赛®是1987年FDA第一个批准上市的低分子肝素,所以在所有低分子肝素中临床循证证据是最多最全面的,并且针对各种特定疾病亚型的患者也进行了高质量的临床研究。例如大家比较熟悉的ESSENCE和TIM111B研究,促进指南对克赛®治疗UA/NSTEMI给出IA类推荐。STEEPLE研究,证实了克赛®在PCI患者中应用的疗效和安全性。而STEMI领域的里程碑研究EXTRACT-TIMI25,促使克赛®获得FDA批准用于STEMI治疗。
心血管网:在临床中有哪些疾病更适合用依诺肝素治疗? 李玉珍教授:基于克赛所进行的大量高质量临床研究已明确,对于稳定/不稳定型心绞痛、ST段抬高/非ST段抬高心梗的患者,依诺肝素都是理想的选择。同时,依诺肝素也可以用于内科治疗中的VTE预防及肺栓塞的部分治疗,临床应用时应注意,这两个单独的适应证是其他低分子肝素所不具备的。所以临床医生在治疗工作时应根据患者疾病特点、个体化需求选择用药,并且依据循证证据指导临床实践,最终作出合理选择,规范应用。
心血管网:您刚刚也提到低分子肝素来源于普通肝素,关于低分子肝素在临床应用中所存在的共性和差异性,请您再给大家解释一下好吗? 李玉珍教授:虽然低分子肝素均是由普通肝素降解而产生,但不同的母代肝素可分离出不同的低分子肝素,且影响最终的低分子肝素的组成成份。而且不同生产工艺可以使普通肝素解聚得到独特的内部及外部端基结构。克赛®是将来自猪肠黏膜的肝素苯甲基酯进行碱性降解而制得的低分子肝素钠盐;其化学结构在目前已经批准的低分子肝素中是独特的,主要特征在于独特的多糖序列和被称为“指纹图谱”的结构修饰,这种独特的结构对生产工艺高度敏感。现在随着分析技术领域的进展,这些指纹图谱的再认识已经成为可能,特殊的制造工艺使得依诺肝素具有独特性,是不可仿制的。这一结论已经得到权威机构和指南的明确肯定。这次SFDA批准克赛通用名由“低分子肝素钠”改为“依诺肝素钠”,也从另一个方面强调了低分子肝素之间的差异性,不能一概而论。 心血管网:随着生物医药技术的发展,一些学术概念的定义也日渐得到重视和更为精确地区分。“相似生物医药制品”和“仿制医药产品”这两个药学概念是目前实践应用中较难区分的,在此,请您给我们讲解一下二者的区别?您认为该如何正确理解二者的内涵以及在临床应用中的实践意义? 李玉珍教授:随着医学和药物研究的发展,新药研发成果显著。但是,新药研发巨大的资金和时间投入,促生了“仿制医药产品”上市。但是,“相似生物医药制品”并不是“仿制医药产品”,人用医药产品委员会公布的关于“相似生物医药制品”的指导原则已明确指出:相似生物医药制品不认为是仿制医药产品。并强调:除了需要对比研究证实其相似的安全性和有效性之外,还必须充分表征其产品。相比高度纯化的、生物技术衍生的产品,提取自生物来源的生物物质更不可能做到这些。 抗凝领域常用的依诺肝素是一种生物医药产品,由生物来源材料猪肠肝素制造。目前不能单独完全通过物理-化学试验来表征依诺肝素,并且其性质取决于物理-化学和生物学试验以及生产方法和控制的结合。已有研究证实依诺肝素1,6-脱水环结构和其他结构指纹图谱可能是其药理学特性和临床特性的基础。此外,依诺肝素不仅通过与抗凝血酶III相互作用起效(占20-30%),而且还可以通过释放组织因子通路抑制剂(TFPI)、与肝素辅因子II(HCII)相互作用、抑制白细胞促凝血作用、促进纤维蛋白溶解、蛋白质结合和调节血管内皮作用等通路起效。这些数据证实抗-Xa/抗-IIa比值等传统LMWH标志不能完全表征类似依诺肝素的LMWHs的整体药理学活性。因此,仅基于“某一产品是参比产品的仿制药形式的一份说明”的标准简化上市许可证申请对生物医药产品是不充分的,声称“类似依诺肝素”产品的申请必须包含适当的临床前试验和临床试验结果。 欧盟理事会、FDA、美国心脏病学会、欧洲心脏病学会等权威机构已形成共识——不同的生物制剂产品之间是不能互换的。提示在临床选择药物时,应牢记不能仅凭仿制产品声称具有与依诺肝素相同的分子量、抗因子Xa或抗因子IIa活性,和/或抗Xa/抗IIa比值,就认为二者具有相同的药理学活性、相同的疗效和安全性。目前,克赛®在全球126个国家得到应用,占低分子肝素类60%的份额,然而,在中国药学学术概念的精确化还有待进一步的学习和提高,所以我认为有必要提出来让更多的临床医生予以重视。
目前,全球低分子肝素药物的主导品牌为依诺肝素钠(Lovenox)、达肝素钠(Fragmin)、那曲肝素钙(Fraxiparine)、亭扎肝素钠(Innohep)。其中依诺肝素钠由全球第四大制药公司法国Sanofi-Aventis(赛诺菲—安万特)生产,达肝素钠由全球第一大制药公司美国Pfizer(辉瑞制药)生产,那曲肝素钙由全球第二大制药公司英国GlaxoSmith Kline(葛兰素史克)生产,亭扎肝素钠由世界知名医药公司丹麦Leo(利奥)生产。依诺肝素钠世界卫生组织、美国药品食品监督管理局、美国胸科医师学会等机构均提出不同的低分子肝素应视为不同的药物,临床适应证不能互相替换。依诺肝素是全球研究最充分、循证医学支持最多的低分子肝素,临床应用以来先后有十个以上的高质量临床研究,所有研究不仅证实患者无论是在介入还是保守治疗应用依诺肝素临床净区益大于普通肝素。依诺肝素(商品名克赛),Enoxaparine,Lovenox,赛诺菲-安万特公司1993年美国上市,专利保护到2012年,是该公司最畅销的药物。2010年7月Sandoz与Momenta制药公司联合开发仿制药依诺肝素钠制剂在美国上市。我国由杭州九源基因工程有限公司2006年仿制上市。2003年克赛进口中国。此外,虽然低分子肝素已占据肝素类药物市场的主导地位,但由于其在血液保存、心脏手术、肾透析、抗动脉血栓、静脉给药留针等传统抗凝血临床应用上无法替代标准肝素,因此,标准肝素仍然具有一定的市场增长空间。目前,全球主要的标准肝素制剂生产企业为美国的APP公司、Baxter、Hospira以及欧洲的Ratiopharm、Sandoz等公司。
2010年赛诺菲的伊诺肝素(低分子肝素钠)在中国销售2.16亿欧元,增长36.6%。
杭州九源亿喏佳,唯一国产依诺肝素钠注射液------亿喏佳采用预填充式注射器,并具有工艺专利------亿喏佳符合欧洲药典6.0及英国药典2000标准,和进口依诺肝素具有生物等效性
虽然低分子肝素类产品的整体价格在逐渐下降,但与普通肝素相比低分子肝素类产品价位仍然较高。较高的价格并未能成为其推广的障碍,这可能是由于应用低分子肝素无须特殊设备,无须监测,可减少住院天数,减少出血合并症等不良反应,并有可能减少心脏事件的发生,因此使用低分子肝素并不一定增加病人的整体费用负担。另外,无须监测抗凝血性比值(INR)的优点使许多不具备监测条件的医院或者社区医院也能让有适应证的病人接受充分的抗凝治疗。
■那屈肝素钙独占鳌头
2006年进入样本医院市场的低分子肝素类药物共有6种,分别为那屈肝素钙、依诺肝素钠、低分子肝素钙、达肝素钠、低分子肝素钠、帕肝素。
那屈肝素钙的医院购药金额排序第一。那屈肝素钙具有因子Ⅹa活性,对凝血酶及其他凝血因子影响不大。其选择性抗凝血性比值一般为1.5~4.0,而普通肝素仅为1左右。该品避免了使用含钠离子的低分子肝素使血液中钠离子浓度增高从而引起血压升高的不良反应。2006年前3季度那屈肝素钙的销售额为3025万元,占据医院低分子肝素类药品28.46%的市场份额。
依诺肝素钠销售额排序第二位,该品为样本医院购入的低分子肝素类产品中增长速度最快的品种。依诺肝素钠是由法国安万特公司研制开发的一种新型抗凝药物,于2004年10月获得美国FDA批准上市,专利保护在2012年结束。2006年前3季度依诺肝素的销售额为2592万元,市场份额为24.38%,较去年同期增长34.80%。
低分子肝素钙排序第三位,市场份额为19.72%,增长率为10.94%。达肝素钠和低分子肝素钠分列第四、第五位,市场份额分别为16.42%和10.97%,二者的销售额均较去年有所下降。帕肝素排序第六,因市场份额较小,仅占低分子肝素市场0.05%的份额,且由于2005年的销售额为零,无法计算其增长率,故帕肝素的销售情况未在气泡图中体现。
2006年前3季度排序第一位的品牌为英国葛兰素史克集团生产的商品名为速碧林的那屈肝素钙。作为世界第一个问世的LMWH,“速碧林”是最早进入中国市场的低分子肝素产品。“速碧林”还是市场上惟一附有安全套装的LMWH,独特设计更多地考虑到了医护人员与家属的安全。“速碧林”不但有多种浓度剂型,还有大包装剂型和浓缩剂型独特的系列产品,这些都方便临床选择,促进其在临床应用上的推广。2006年前3季度“速碧林”的市场份额为28.46%,增长率为7.79%。
排序第二位的为浙江杭州赛诺菲圣德拉堡民生制药公司的商品名为“克赛”的依诺肝素钠。依诺肝素钠是目前赛诺菲-安万特销量最好的药物,2006年上半年该产品的全球销售额为12.4亿欧元,其中7.65亿欧元来自美国市场。2006年前3季度“克赛”在信息网样本医院市场所占的份额为24.38%,增长率为34.80。
样本医院低分子肝素市场大部分被“速碧林”和“克赛”所占据,排序第三位的“博璞青”等品牌的市场份额已经降到9%以下。
表1:2006年前3季度排序前5位的品牌
■期待新剂型问世
国内外临床上应用的LMWH剂型主要为注射剂。注射剂有疗效确切、易吸收、起效迅速等优点,但它的半衰期短,对需要长期用药者不便。因此开发方便给药与延长半衰期的剂型前景诱人。
目前尚无口服制剂应用于临床的报道。美国的一项临床前研究中,给灵长类动物口服Elan公司的LMWH,生物利用度相当于皮下注射给药的38%,灵长类动物口服LMWH耐受性良好。
根据LMWH具有活血化淤、抗炎、止痒、止痛等药理活性,可用于治疗冻疮、皲裂、软组织挫伤、血肿、烧烫伤、浅表血栓静脉炎以及昆虫叮咬等造成的局部炎症的特点,齐鲁药厂研制出LMWH钠凝胶。他们以卡波姆为凝胶基质,加入透皮吸收促进剂,体外透皮量及体外透皮吸收动力学研究显示,LMWH钠凝胶比普通肝素钠软膏具有更多的优点。
临床上应用的肝素类化合物透皮吸收制剂多为软膏或凝胶,只能在局部发挥改善局部血液循环、消肿去瘀等作用。近年来,研究表明,脂质体可以包封难以透皮的药物及易在胃肠道被破坏的生化高分子药物,促进其透皮吸收,发挥全身治疗作用。
迄今为止,国内外对LMWH的剂型已经进行多方面的探索,比如胶囊剂、软膏剂、脂质体、类脂质体、前体脂质体、脂质体喷胶、柔性纳米脂质体、明胶复合物、肺靶向微球等,各种剂型均有各自的特点,但目前这些工作仅限于实验室探索阶段。
自20世纪70年代低分子肝素(LMWH)发明以来,由于其具有优于普通肝素的良好的抗血栓作用和较低的抗凝血作用,在临床抗凝治疗中得到广泛的应用并取得了良好的效果。但是,对于肝素在非抗凝方面的作用,却鲜为人知。本文仅就LMWH在非抗凝作用方面的部分进展予以综述,供读者参考。1、 在产科及妊娠方面的作用选择有正常月经周期、身体健康、无子宫腺肌病和子宫内膜异位症良性子宫脱垂或子宫肌瘤患者行子宫切除取子宫内膜组织样本,将子宫内膜间质细胞与黄体酮和17β雌二醇共同进行培养蜕膜,同时分别加入人凝血酶、人FXa、普通肝素(UFH)、硫酸葡聚糖、及4种不同商品的LMWH进行培养,用ELISA方法在第3天检测胰岛素样生长因子(IGF-I),第12天检测重组人胰岛素样生长因子结合蛋白1(IGFBP-1)和催乳素(PRL)浓度,结果发现,凝血酶和FXa与单用激素刺激相比,明显增加了IGF-I的分泌,硫酸葡聚糖和肝素同样可以刺激IGF-I和PRL而抑制IGFBP-1,表明肝素对子宫内膜间质细胞的作用是不依赖其抗凝作用而独立的,UFH和不同商品的LMWH比较也具有相同的作用,只不过LMWH的作用略低于UFH,且IGF-I的分泌与肝素呈剂量依赖效益,有趣的是,这种剂量依赖性即使是在超生理剂量的肝素下,其IGF-I的分泌也是一个常数,这表明肝素对人子宫内膜的作用是一个直接的效益而不是通过交互分子形成复合物发挥生理效应的[1]。Noble等[2]分别对照观察25例用LMWH和25例用UFH并加用小剂量阿斯匹林治疗抗心磷脂抗体综合征(ASP)伴妊娠妇女,结果发现,LMWH组流产率为14%,UFH组为20%,表明LMWH和UFH在预防ASP妊娠患者流产方面具有相同的作用;经典的补体通道和激素免疫系统相关,研究发现[3],在LMWH和C1亚单位C1q之间具有介导作用,要比起始时对抗X因子活性4倍增高,结果显示LMWH和C1q之间的介导作用不但具有独立的作用而且也具有独立的抗炎和防止流产的作用。但是Berker等[4]将连续两次卵泡内单精子注射-胚胎移植术(intracytoplasmicsperm injection and embryo transfer,ICSI-ET)失败的患者分为2组,一组以LMWH治疗,可供分析病例104例,另一组为对照组,可供分析病例为103例。LMWH治疗在胚胎植入后12到14天,妊娠试验阳性则持续使用到妊娠第12周,如果阴性则停止治疗。结果发现,LMWH组其临床妊娠率(CPR)、活产率(LBR)、着床率和多胎率分别为34.6%、30.7%、22.6%和41.6%,对照组则分别为33.9%、29.1%、21.1%和42.8%,两组比较没有显著差别。而对于3次及以上植入失败(RIF)患者的CPR、LBR、着床率和多胎率在LMWH组(n=48)对照组(n=43)分别为35.4%、31.2%、21.1%、23.5%和27.9%、23.2%、15.8%、25.0%,虽然比值较高,但仍然无统计学意义。这项研究否认了LMWH在多次RIF患者的治疗效益。将72例均有严重的妊娠并发症和胎盘血管病变患者进行回顾性对照研究[5],实验组即LMWH组32例和对照组非LMWH组40例,结果显示,LMWH组严重的先兆子痫、胎儿生长限制(FGR)、大于20周的胎死率、胎盘早剥的发生率以及总体不良结果分别为3.13%、6.25%、0%、0%和9.4%;对照组则分别为20%、22.5%、2.5%、15%和60%,除FGR和大于20周胎死率外,其他结果均具有显著的区别。这些结果提示,用LMWH治疗的妊娠妇女,可以有效地减低严重的胎盘早剥和先兆子痫的风险。先兆子痫与胎盘蛋白13(PP13)具有相关性,PP13是β半乳糖苷结合的S型半乳糖凝集素家族成员之一,只在高级灵长类动物的胎盘组织表达,且仅存在于绒毛膜滋养层的多核合体滋养细胞中,PP13表达并释放到绒毛间隙而进入母体血液循环。正常妊娠从开始到妊娠后期,PP13的血清浓度是增高的,而当孕妇出现先兆子痫开始时,其PP13在第一孕期低于正常,随后,当临床症状进展时,PP13又高于正常,这种现象在妊娠中期交替发生。但Grimpel等的研究结果表明LMWH与PP13无相关性[6]。2、 对肿瘤及肿瘤转移的作用荟萃分析[7]29位作者进行的38项关于肝素/低分子肝素对癌细胞肺转移影响的实验,38项实验包括将人、兔或鼠的乳腺癌、黑色素瘤、结肠癌、肺癌、鳞状细胞癌和骨肉瘤等肿瘤细胞注射入小鼠体内,再将不同剂量UFH/LMWH在肿瘤细胞注入前24小时至后24小时的不同时间内予以静脉、皮下或腹腔注射,观察肝素对癌细胞肺转移的影响,结果显示38项55组试验中,仅有6项8组实验无影响,其余32项42组实验均显示肝素降低了癌细胞的肺转移作用,而且其作用呈时间和剂量依赖关系[7]。进一步的研究证实肝素抗癌转移的生物学机制与抑制肝素酶、阻断P-和L-选择素介导的细胞黏附作用以及抑制血管增生有关。P-选择素主要大范围地结合肝素硫酸和肝素片段,而L-选择素可能需要和更特定的序列相识别,虽然在粘蛋白样分子上结合的唾液酸路易斯X模式(Sialyl-LewisX motif)被认为是选择素之间的一个共享配体(sharedligand),但其交互作用却十分微弱,这个结果提示肝素-选择素交互作用的机制涉及积聚阴离子补丁(clustered anionicpatch)而不是线性的寡聚糖序列(a linear-definedoligosaccharide)[8]。此外,LMWH还可以干扰整合素α4β1(VLA-4)与VCAM-1的交互作用并抑制VLA-4的交互作用,通过血小板整合素αIIbβ3介导而抑制黑色素瘤细胞-血小板之间的交互作用,抑制凝血酶依赖的蛋白酶激活受体1(PAR1)的活性,从而进一步抑制血小板和内皮细胞活性以及L-和P-选择素介导的细胞-细胞间的粘附作用。CD24作为P-选择素的配体,也参与肿瘤的转移,LMWH抑制P-选择素/CD24之间的交互作用,以防止血小板对肿瘤细胞的黏附作用[8]。同样,在研究LMWH对肿瘤转移的影响时[9],将肺癌细胞通过小鼠尾静脉注入小鼠体内,制成肿瘤转移的动物模型,并将其分为对照组、多配体聚糖组、LMWH组和LMWH+多配体聚糖组,实验14天后,将小鼠处死,解剖其肺组织,观察肺肿瘤灶的形成,结果发现,对照组和多配体聚糖组的肺肿瘤灶的形成明显高于LMWH组和LMWH+多配体聚糖组,表明LMWH有抑制肺癌细胞转移的作用,其机制可能和内皮细胞多糖有关,由于肝素多糖的硫酸乙酰肝素链导致了实验性肿瘤转移的下降,另外,LMWH通过竞争性地与肝素酶或透明质酸酶结合,保护了这些酶对于血管内皮及其屏障功能的损害,从而抑制了肿瘤的转移。另外,将黑色素瘤和胰腺癌瘤细胞混合培养后注入仓鼠体内生长,形成瘤块后再植入大鼠皮下制成动物模型,共46只大鼠,其中23只皮下注射LMWH200IU,另一组23只为对照,10天后分别观察其微血管的数量(N)和长度(L)、血管面积分数(AF)、红细胞速度(V)、微血管密度(MVD)、血管分形维度和血管周细胞覆盖指数(PCI),结果发现,对照组的N、L和AF均有显著增生,而LMWH组N、L无明显变化,AF显著减少;两组的V在初始阶段是增加的,但是LMWH组随时间推移会出现一个早期的下降;MVD和血管分形维度是显著的减少,而PCI却明显增高。提示LMWH可以抑制肿瘤的血管增殖导致微血管的正常化[10]。然而,Vivarelli等[11]对229例肝硬化并发肝癌患者行小肝叶切除术,一组157例病人用LMWH预防血栓形成治疗,另一组72例病人未用LMWH治疗,结果显示,与使用LMWH组比较,在未用LMWH组,模型终末期肝病积分(modelfor end-stage liver disease,MELD)和手术期平均血浆输注量均明显增高,而血小板计数、食管静脉曲张的发生率却显著降低,通过对静脉血栓和出血并发症的多因素分析发现,只有食管静脉曲张具有高出血的危险风险,而两组病人的血栓性危险因素如体重指数(BMI)、糖尿病和心血管疾病的发生以及出血性疾病的发生均无显著差别。因此,作者认为,除非有大宗病例研究得出的临床指南性的标准,否则,对于具有这类高出血危险病人在外科手术时是否有必要预防性使用LMWH,需要慎重。3、 对血管增殖与血管内皮的作用血管内皮生长因子(VEGF)在胚胎期的血管生成和新生以及成人的新生血管生成方面具有极为关键的作用,天然的VEGF抑制剂如可溶性VEGF捕获受体Flt1(solubleVEGF-trapping receptorFlt1,sFlt1)sFlt1参与了VEGF的调控作用,无论是VEGF降低还是sFlt1升高,都会涉及到临床上某些疾病如先兆子痫的病理生理过程。硫酸乙酰肝素(HS)蛋白多糖可以结合sFlt1分泌细胞,sFlt1各亚型是极好的肝素结合剂,这种强力的与肝素结合的能力可能影响其生物活性。sFlt1的主要分泌场所是主动脉弓和胎盘绒毛膜细胞。Yagel等[12]用LMWH预防孕妇凝血功能障碍的风险,发现应用LMWH孕妇血清sFlt1的水平要明显高于未用LMWH孕妇,但有趣的是,使用LMWH孕妇,其VEGF水平也有比sFlt12-4倍的升高,表明机体具有保障VEGF/sFlt1比值的生理反应。进一步的研究[12]发现,HS与sFlt1结合,形成sFlt1-HS复合物,沉积在胎盘组织,当加入肝素酶时,由于肝素酶对HS链的剪切,使sFlt1从胎盘中释放增加。比较未妊娠的野生型小鼠与过表达肝素酶转基因小鼠(HTG),发现HTG小鼠血清sFlt1水平要比野生型小鼠超过2倍增高;妊娠的野生型HTG小鼠其差别更为显著,且随妊娠晚期呈指数性增高。当肝素酶在胎盘绒毛细胞被中和后,sFlt1与对照组比较其分泌降低35%。这些研究结果表明LMWH具有增加sFtl1从而抑制VEGF的作用。Norrby等[13]分别用单用LMWH、表阿霉素和两药联合处理大鼠,并测量其平均微血管扩展空间(VA)、微血管长度(MVL)和总的微血管长度(TMVL,VAXMVL)以观察药物对肿瘤血管增殖的作用,结果发现,LMWH单用对血管增殖的刺激作用与剂量呈反相关,表阿霉素对血管增殖无有意义的作用,而LMWH加表阿霉素对血管增殖具有显著的抑制作用。这个结果表明,LMWH在活体条件下具有促进血管形成的效用,而LMWH联合表阿霉素却可显著地抑制血管增生,提示活体条件下血管抑制作用是一个药物的复合效益。Park等[14]将LMWH与脱氧胆酸(DOCA)进行共轭交联形成LMWH衍生物LHD,根据LMWH与DOCA的配比比例不同,依次递增,合成LHD1、LHD1.5、LHD2和LHD4,分别将上述药品作用于鼠鳞状细胞癌(SCC7)接种的小鼠以及SCC7和A549(人肺癌细胞)细胞系,结果发现,对细胞活性LMWH及LHD各组均无明显影响,表明与LMWH相比DOCA无明显增加细胞毒的作用;无论肿瘤体积、肿瘤重量以及微血管增生等,LHD4均较其他各组具有明显的抑制作用,且与剂量呈正相关而抗凝作用几乎为零。将275例经血管造影或超声检查股腘血管超过50%病变患者用经皮腔内血管成形术(PTA)治疗后,随机分为两组,分别用阿司匹林和阿司匹林加LMWH进行预防血管再狭窄,观察血管再生重建和临床外周血管性病变(如跛行、休息痛、坏疽性溃疡等),结果发现,血管狭窄发生率在LMWH组为44%,对照组为50%,无显著性区别,严重的外周血管病变发生率分别为43%和41%,而在严重的肢体缺血患者血管再生LMWH组较对照组显著降低,分别为45%和72%[15]。Rectenwald等[16]研究LMWH对肺动脉损伤的作用,将实验大鼠用硅做成肺栓塞模型,皮下注射LMWH治疗,21天后获取鼠肺组织,检测总胶原蛋白(totalcollagen),单核细胞趋化蛋白-1(monocyte chemoattractant protein-1,MCP-1),白细胞介素13(interleukin-13,IL-13)和转移生长因子β(transforming growthfactor-β,TGF-β)。结果发现,所有肺栓塞者均可以使PaO2明显降低,与对照组相比,硅栓子组(the siliconeemboli group)在第1天、第4天和第14天,其IL-13、MCP-1和所有的炎性介质(all inflammatoryMediators)分别明显增高;伴随这些不同差异,与对照组相比,硅栓子组在第4天和第21天其肺动脉内膜均显著增生,而肝素治疗组其IL-13水平在任何时间都是降低的,TGF-β在LMWH治疗组的第4天和14天也是显著降低的,另外,与对照组和其他治疗组(tPA、gIIB/IIIA拮抗剂阿昔单抗(abciximab)处理鼠)比较,只有肝素治疗组在第14天其肺动脉内膜增生是降低的。这些结果证明,由惰性物质导致的持续的肺动脉扩张可产生与血栓无关的显著的炎性反应和内膜增生。与未治疗的PE组相比较,LMWH是唯一具有与显著减少晚期内膜增生,TGF-β以及低纤维化生长因子生成相关的治疗作用的药物。因此,临床上,对于肺动脉栓塞应尽早使用LMWH进行治疗,以便于最大限度地减少损伤反应以及与此相关的持续的肺动脉阻塞。4、 对脂代谢的作用对20例慢性血液透析(HD)患者,分别使用UFH和LMWH,观察脂蛋白脂肪酶(LPL)的变化,结果发现,使用LMWH的HD患者,其LPL活性在40分钟和180分钟时增高,经6个月的治疗研究观察,在HD开始和结束时,LPL活性与肝素活性始终存在显著的相关性,表明组织的LPL没有被耗竭;在HD过程中,甘油三酯在LMWH要比UFH高,结论是HD患者使用肝素并不能够消耗LPL系统[17]。Näsström等[18]用LMWH治疗血液透析病人以防止体外凝集,结果发现LMWH对脂蛋白酯酶(LPL)的影响要比普通肝素大。9例患者先用普通肝素(UFH),两周后再用LMWH,分别在用药后的不同时间采集样品,测定血浆LPL、HL(肝脂酶),甘油三脂(TG),胆固醇,高密度脂蛋白(HDL)和低密度脂蛋白(LDL),结果发现,TG,胆固醇,HDL和LDL在两组病例没有显著的差别。但在透析早期阶段(180分钟之前)UFH和LMWH对LPL的影响均不显著,而在透析阶段后期(180分钟之后),血浆LPL的活性明显下降,而LMWH较UFH更为显著,6mU/mlvs22mU/ml(180分钟)和5mU/mlvs11mU/ml.LPL活性的平均曲线下面积(AUC)在透析早期两者无显著差别,而在180~240分钟,LWMH的AUC明显低于UFH。另外,将60个平均透析时间为4.15±0.52年的血液透析病人分为2组,一组27人,用普通肝素预防,另一组33人用LMWH预防,平均年龄为58.54±2.24岁,研究观察时间为12个月,结果发现,与标准普通肝素比较,LMWH可以显著降低高密度脂蛋白胆固醇,而对低密度脂蛋白胆固醇则没有显著区别,同时,LMWH在系统灌注和透析液也比UFH有较好的效果,LMWH在女性透析患者可使其血脂得到改善,而男性患者用UFH在头6个月的抗凝作用要优于女性患者,无论是UFH或LMWH其平均血液凝块率下半年比上半年都有显著的下降,且UFH要比LMWH下降的更为显著[19]。但是,Katopodis等[20]分别将6个血液透析、腹膜透析和健康对照者分成2期,用UFH和LMWH治疗,分别在用药后的1、2、3和4小时测定其总胆固醇、甘油三酯、高、低密度脂蛋白等,结果发现,在所有试验组的2个治疗期,均只有甘油三酯降低而其他的脂蛋白并不受到影响。5、 对骨代谢的作用用UFH和LMWH处理鼠破骨细胞的作用时发现[21],标准剂量的UFH(0.1-10U/ml)和LMWH(1-100抗XaIU/ml)可以发生两个方向的变化,在低剂量时,可以导致大鼠破骨细胞形成增加,在高剂量时(UFH10U/ml,LMWH100抗XaIU/ml)则导致破骨细胞的形成减少;而在小鼠的骨髓培养中,肝素却抑制了破骨细胞的形成。这个机制可能与肝素蛋白结合的能力有关,通过与肝素高度的亲和性,肝素可以保护某些生长因子的特性,肝素与骨基质结合,介导了细胞类型在骨微环境中的变化,包括与成骨细胞系细胞的交互作用,释放生长因子和细胞因子,从而诱导单个核前体多能干细胞在骨微环境中形成破骨细胞。另外,肝素可以增加IL-11诱导RANKL在小鼠颅骨细胞的表达,表达RANKL的成骨细胞在M-CSF条件下,形成成熟的破骨细胞。资料显示,达纳肝素可以抑制成骨细胞的增值、蛋白合成以及降低骨钙蛋白和碱性磷酸酶的水平,与此相反,磺达肝素(fondaparinux)却没有其效应。将成骨细胞暴露于磺达肝素中,显示出线粒体的活性和蛋白的合成要比未暴露于磺达肝素中显著增高。与此相反,肝素、达纳肝素或伊诺肝素的治疗相关的浓度可以降低成骨细胞基质胶原蛋白II型的含量和钙化,而磺达肝素缺乏相应的作用[22]。然而,Lefkou等[23]系统回顾有关LMWH对骨骼的影响发现,普通肝素所致骨质疏松性骨折的发生率约为2.5~5%,而LMWH却比较罕见且缺乏相应的危险度分析。对长期使用LMWH(时间超过3个月)的患者进行文献资料复习,结论很难统一,文献复习中,基本上都是个例报告,作者最认可的由LMWH诱导的骨质疏松性骨折或系统性骨质疏松病例总共仅11例,其中有8例为妊娠期患者。(有两例报告长期使用LMWH导致严重骨质疏松,)另外,一组最大宗的妊娠患者使用LMWH的资料系统复习显示,包括64组研究报告的2777例妊娠患者,仅有1例骨质疏松性骨折,占0.04%;另一组系统复习的728例妊娠患者,有2例报告发生骨质疏松性椎体骨折。通过测定骨密度(BMD)比较长期使用UFH和LMWH的作用,发现,使用LMWH的49例患者中有1例(2.3%)发生有意义的骨密度降低,而UFH组的40例无一例发生骨质疏松。在一个随机开放的实验中,44例妊娠患者,被随机分为两组,一组21例使用LMWH,另一组23例使用UFH,同时与一组19例正常人做对照,在妊娠和产褥期使用肝素治疗预防血栓事件发生,在第1、6、16和52周(如有可能在3年后)测量BMD,结果显示,UFH组在腰椎骨密度减低要显著低于LMWH组和正常对照组,LMWH组和正常对照组没有显著区别。另外一组研究比较长期使用LMWH与香豆素预防继发性血栓时患者的骨密度变化,结果发现,在3~24个月的观察过程中,15例使用那曲肝素和42例使用依诺肝素患者与29例使用香豆素的患者比较,在第1和第2年的随访中,其股骨的BMD的降低率平均分别是3.1%对1.8%和4.8%对2.6%。因此,从这些研究的报告中,目前很难得出LMWH确实有诱导妊娠患者骨质疏松的结论。6、 对细胞凋亡的作用将谷氨酸与大鼠脑皮质细胞联合培养,观测其诱导皮质细胞的凋亡作用,发现用谷氨酸处理的鼠皮质细胞其凋亡率增加33.21%,谷氨酸处理皮质细胞24小时后其[Ca2+]浓度增加,Bcl-2表达下调,Bax表达上调,半胱氨酸天冬氨酸蛋白激酶3活性增加,在加入超低分子肝素(ULMWH)后,无论是结合钙还是游离钙增速均减缓,上调了Bcl-2的表达,下调了Bax的表达和半胱氨酸天冬氨酸蛋白激酶3的活性。表明ULMWH具有通过Ca2+的释放,修饰细胞凋亡过程而保护神经细胞的作用[24]。同样,Deepa等[25]研究阿霉素和LMWH对大白鼠心脏和肾脏的药理作用也得出了相同的结论,实验鼠一组单用阿霉素,一组在注射阿霉素后一周再使用LMWH,结果发现单用阿霉素组与对照组相比在心脏和肾组织的反应性氮核素(reactivenitrogen species,RNS)分别增高1.51倍和2.36倍,TNF-α分别增加2.4倍和7倍,DNA电泳也出现标准的凋亡梯带;而加用LMWH组的RNS、TNF-α均基本恢复至对照组水平,细胞凋亡电泳带消失。这些结果证明,LMWH具有良好的抗阿霉素诱导的心肌和肾组织细胞凋亡的作用。另外,Kukner等[26]研究LMWH对肝脏细胞的保护作用,将30只小鼠分为5组,分别是对照组,橄榄油加CCL4组,CCL4加LMWH组,LMWH组和橄榄油组,试验4周后取肝组织,通过组织化学染色及细胞免疫等方法观察肝细胞的增值和凋亡活性,结果发现CCL4可以导致肝中央静脉周围肝细胞明显的坏死,以及炎性细胞和肥大细胞的增值;肝细胞脂滴沉积、肝糖原降低、细胞凋亡、核肿胀等,而LMWH可以使受CCL4损伤的肝细胞的坏死、凋亡和肥大细胞的数量显著减少,但并不影响肝细胞脂滴的沉积。因此,LMWH可以有效地降低CCL4对肝细胞的早期损害。7、 抗炎性作用通过研究肝素对马蹄板炎的作用发现,肝素可以显著地抑制马中性粒细胞髓过氧化物酶(MPO)的活性且呈剂量依赖型,而且最高的LMWH浓度可以产生最高的MPO抑制作用。MPO的捕获在动脉细胞较高,但肝素的抑制作用在静脉细胞更显著,这些结果表明,肝素具有抑制炎性反应的作用,UHF与LMWH二者之间无显著的区别[27]。Luo等[28]将LMWH制备成口服结肠缓释剂型,观察LMWH对小鼠溃疡性结肠炎的效应,研究者共分6个实验组,每组20只小鼠,分别为模型对照组、赋形剂对照组、达肝素钠治疗组、依诺肝素治疗组、普通肝素治疗组和5-氨基水杨酸治疗组。在体内和体外观察结肠组织学变化、血清TNF-α、IL-6、FXa以及结肠Musashi-1表达(一种肠肝细胞标记物),结果发现,口服含LMWH的结肠特异性缓释胶囊的小鼠,可以显著降低在肉眼和组织学观测下的结肠炎的特征,可以显著降低TNF-α、IL-6以及FXa的血清学水平,显著提高Musashi-1在结肠的表达。这些结果表明,口服的LMWH具有潜在的治疗炎性肠病的作用。对84例进展期肝炎肝硬化患者予以LMWH治疗并研究其相关指标,结果显示,84例患者中有7例由于食道静脉曲张和高血压胃病发生出血并发症,但无因出血死亡病例,无血栓事件发生。抗凝血酶III(AT)与抗Xa活性呈正性相关,AT与儿童肝功能分级(CTD分级)呈负相关,而凝血前因子如凝血酶原时间和血小板计数则和抗Xa无关,抗Xa与病人的体重质量指数(BMI)、腹水状况呈负相关,AST/ALT、胆红素、血糖和血脂等与抗Xa无相关性。这些研究资料显示,肝硬化病人使用标准剂量的LMWH治疗,并不能够达到推荐预防或治疗剂量的抗Xa水平,用CTD或MELD积分评定,抗Xa水平与肝硬化疾病的严重程度呈负相关,AT水平与抗Xa值呈正相关,表明肝合成功能的直接作用,特别是在LMWH作用下,AT作为一种监测工具可以准确地检测到标准抗Xa活性。总之,LMWH在肝硬化的应用是安全的,但是,标准剂量显得太低以至于不能够产生足够的抗Xa活性的作用,最有可能的原因是由于溶解量的增加和AT的合成受到损害。但如何平衡出血风险和抗凝效益还需要作进一步的研究[29]。8、 其他Haim等[30]报告一例早熟新生儿并发呼吸道疾病,予以LMWH 治疗,出现FT4增高,停用LMWH后FT4恢复正常。由于肝素导致脂蛋白脂肪酶释放,引起血浆游离脂肪酸增加,从而导致甲状腺素从其结合的蛋白上离析出来,使游离甲状腺素增加,这种增加的甲状腺素不会引起甲亢的症状也无须治疗。此前,Stevenson等[31]将9个健康男性志愿者(年龄33~54岁)和19个心脏病患者(男13人,女6人,年龄42~87岁)进行对照性研究,主要观察皮下注射LMWH的生物作用,分别在注射肝素前、注射后3小时、24小时和48小时抽血检测其FT4、血脂等并比较其变化,结果发现,9名健康志愿者,在注射肝素前后无论是游离脂肪酸、FT4还是TSH本身并无显著的变化,但是游离脂肪酸、甘油三酯与FT4的浓度变化却有显著的相关性;然而,对于住院的心脏病患者,在注射LMWH后2~6小时,10个病人中有4个患者的游离脂肪酸和FT4显著增加,进一步的观察,18例患者在注射肝素后10小时,其FT4轻度增高,而游离脂肪酸显著增高,且均要高于健康志愿者水平。这些结果提示,LMWH具有增高FT4的作用,而这个生物效应可能与游离脂肪酸的释放有关。为研究LMWH对肾-血管紧张素-醛固酮系统的影响,将30个研究对象分为3组,每组10人,分别为糖尿病肾病患者组、非糖尿病肾病患者组和健康对照组。分别予以LMWH每天4000IU,皮下注射,研究观察时间为11周。测量肾血流动力学、肾小球滤过率、肾血浆流量、平均动脉压和心率等指标,结果发现,LMWH无论在盐摄入组或限盐组,均不能够影响血管紧张素II诱导的肾血流动力学的改变,也不能够降低醛固酮的水平,肾小球滤过率在所有研究小组均无变化;然而,LMWH在糖尿病肾病组却可以显著地降低蛋白尿[32]。Thomas[33]等观察一例老年糖尿病患者使用LMWH,导致高血钾症。认为与醛固酮抑制有关。总之,无论是普通肝素还是低分子肝素,除了其人们熟知的抗凝作用外,还具有许多的非抗凝效益,这些非抗凝的作用以及可能还存在的我们尚未知的其他药理作用,是需要我们积极关注和探讨的。
关于低分子量肝素类药品的审评思考时间:2010-11-30 09:05来源:审评四部 作者:陆益红、赵慧玲、余立 点击: 248 次
低分子肝素(low-molecular-weightheparin,LMWH)是一类以未分级肝素为起始物料经过分级或降解而得到的具有较低分子量的低聚糖混合物。它具有抗Xa活性,可抑制体内、体外血栓和动静脉血栓的形成,但不影响血小板聚集和纤维蛋白原与血小板的结合。
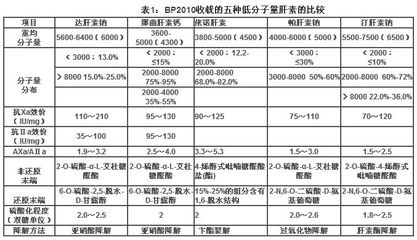
英国药典1993版开始收载了这类品种的通则要求:重均分子量在8000以下,小于8000的级分不少于60%;抗Xa因子与抗IIa因子活性比不小于1.5。随着不同生产工艺的应用,各工艺产品体现出各自的特点,如存在着不同的末端结构、分子量及其分布、抗Ⅹa因子活性、抗Ⅱa因子活性、抗Ⅹa因子与抗Ⅱa因子活性比,其药理作用和临床适应症也有所不同。EP7.0和BP2010收载了5种不同工艺的LMWH,分别是达肝素钠(Dalteparinsodium)、依诺肝素钠(Enoxaparin sodium)、那曲肝素钙(Nadroparincalcium)、帕肝素钠(Parnaparin sodium)和汀肝素钠(Tinzaparinsodium,又名汀扎肝素)。其结构特点与制备工艺见表1。
BP中收载的低分子肝素均分别按细分的品种在正文中体现,目前我国也已有分类的低分子肝素制剂如那曲肝素钙注射液、依诺肝素钠注射液、达肝素钠注射液、帕肝素钠注射液等进口。所以依据仿制药必须遵循“仿制要同,质量一致、临床可替代”的原则,建议企业对照EP那曲肝素钙、达肝素钠和依诺肝素钠的要求以及国外已上市原研发厂产品,根据不同工艺、末端结构、分子量及其分布、抗Ⅹa因子活性、抗Ⅱa因子活性、抗Ⅹa因子与抗Ⅱa因子活性比对LMWH进行分类研究与完善,然后按照相应的注册分类进行申报。同时也建议对国内已上市的LMWH及制剂在一定的时间内根据其工艺等进行细分与质量标准的提高工作。
2.1 DVT治疗方法的选择DVT的治疗方法主要有保守治疗与手术治疗2种。目前较为一致的意见是严重的髂股静脉血栓或全肢型血栓,特别是合并股青肿者,手术取栓越早治疗效果越好[1]。本组686例DVT的预后情况也显示,手术治疗组的静脉通畅率显著高于药物保守治疗组,其远期治疗效果也明显好于药物保守治疗组。手术治疗可彻底取出静脉内血栓,使微循环-小静脉-主干静脉通畅,术后才能够构建有效的动、静脉循环,减少了血栓复发及残留血栓脱落,防止致命性肺栓塞的发生。手术取栓的时机选择一直是一个有争议的问题,目前尚无明确的统一标准。1·1 肝素治疗肝素治疗DVT有着重要和显著的效果,这一结论已经几十年的临床实践所证明。肝素可避免新的血栓形成,并促进病人自身机体纤溶系统的活性来消除血栓[1]。在开始肝素治疗前,应行活化部分凝血活酶时间(APTT)、凝血酶原时间(PT)及血小板计数的检查。适应证:无出血倾向的DVT病人原则上均可应用,特别适合于经济条件差,已明显错过溶栓机会的DVT病人。禁忌证:出血体质、肝素过敏或出现肝素抗体者。溃疡病及流产后不久的病人慎用。 使用方法:主要有静脉持续泵入、静脉间断推注和间断皮下注射3钟。(1)静脉持续泵入:治疗开始时应给予大剂量肝素以阻止血栓进一步生长。首次给予静脉内30~50mg肝素冲击量,接着应用微滴泵每小时持续泵入0·08~0·12mg/kg的肝素。抗凝效果通过监测激活的凝血酶时间(ACT)、APTT而获得。治疗过程中须调整肝素输注速度以保持ACT在200~300s或APTT时间达到对照值的1·5~2倍,至少6h检查一次。ACT检测方法简易,病房内即可操作,且可随时反复监测,但在敏感度和精确度方面比后者稍差。当肝素剂量稳定后,至少每日两次ACT或APTT检查。必须保持最低程度的抗凝水平以使机体获得有效的抗血栓形成状态。抗凝不充分可导致血栓进一步繁衍、复发及肺梗死(PE)的发生[1]。如果APTT保持高于1·5倍对照值,很少发生血栓再发,抗凝达不到这一标准可导致20%~25%的复发率[1]。如果APTT低于对照值的1·5倍,血中肝素水平可通过追加额外剂量及加快输注速度来迅速升高。当APTT持续偏高,肝素输注可短时停止,但不要超过1h。肝素需要量常常在病变发生的头几天最大。(2)静脉间断推注:按0·8~1·0mg/kg体重的剂量一次性静脉推注或输液小壶内滴注肝素,每6h一次,每次给药前行ACT或APTT监测。控制范围同静脉内泵入法。(3)皮下注射:肝素皮下注射已被证明与静脉内肝素同样有效。皮下肝素开始剂量是1mg/kg,每6h一次。在下一次给药前30min行APTT检查,使之达到正常值的1·5~2倍,并以此调整剂量。大量DVT病人在门诊肝素治疗时经验用法为50mg皮下注射,每天两次,主要为替代ACT或APTT的频繁监测。由于更容易精确调控,我们主张应用静脉内泵入肝素的方法标准抗凝。肝素治疗一直到血栓生长完全停止并且口服抗凝药充分起作用时停止,一般5~10日或更长时间。并发症:(1)除了开始阶段为阻止血栓生长而给予大剂量肝素引起出血等并发症外,一般很少发生。严重出血并发症的发生率不足5%[1]。大多数严重出血在肝素治疗开始后的48~72h内发生,这个时间常常是血栓已被控制,肝素需要量正在减少的时候。且多见于老年妇女,术后或有出血倾向的病人中。如果APTT几个小时内均超过对照值的3倍,要小心发生出血,并可适当减少肝素剂量。(2)病人中肝素引发的血小板减少症的发生率在4%~5%[1],而由此并发症引起的血栓发生率为18%~61%,出血并发症不足5%[1]。接受肝素治疗的病人应每日检查血小板计数。如果在治疗过程中,出现血小板计数不足100000/mm3,或血小板计数下降超过50%,并伴有抵抗抗凝的情况,或发生新的血栓,均表明发生了血小板减少症。应停止使用肝素并测定血浆中与肝素相关的抗血小板抗体量(ELISA法)。同时改用华法林抗凝。血小板计数常在2~4天内恢复正常。接受肝素治疗的病人中过敏反应(荨麻疹,支气管痉挛)的发生率不足2%。1·2 低分子量肝素(LMWH)治疗目前,LMWH也已经成功地用于治疗DVT。LMWH具有很强的抗凝血因子Xa的功能,达到防止血栓形成。在各适应证规定的剂量下,不会引起总的凝血方面的明显变化,亦不延长出血时间。与普通肝素相比,血中半衰期明显延长,生物利用度有很大改变,从30%增至90%,作用时间长达24h。对APTT作用极弱,因而抗Xa/APTT活性比肝素大,极少增加出血倾向。LMWH通过皮下给药时具有更长的血浆半衰期,约4h,血小板减少症及过敏的发生率更低。近年来,抗凝研究集中于低分子量肝素[2,3],由于可在门诊病人中使用,非常方便。LMWH与普通肝素有相同的疗效,且大大降低了由于住院及各种血液监测等造成的经济负担。由于此类制剂在国际上还没有统一的标化标准[4],各种LMWH之间在疗效上仍有差异。我们使用Fraxiparine(“速碧林”Sanofi,法国),疗效相对较好,抗凝治疗时0·01mL/kg,12h一次;预防治疗时减至每日一次。由于该剂型有以上的优越性,已逐渐成为我们的主要抗凝治疗药物。1·3 华法林治疗华法林在肝脏内竞争性抑制维生素K依赖性凝血因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ)的生成,从而抑制体内的凝血过程,但其对已合成的凝血因子没有作用。因此,华法林治疗的头3~5天应给予肝素治疗。换句话说,在肝素治疗的中期或开始后不久即应开始服用。华法林的初始剂量为5~8mg/d。维持量以延长PT时间1·5~1·7倍为宜,目前多被国际正常化比值(INR)所替代,即最佳维持剂量应满足INR2~3[5,6]。我们在临床上一般将药物剂量调整到INR2·0即可。在老年及肝功能不全的病人中小剂量常常有效。在达到华法林治疗满意的PT时间段的病人中,出血并发症约4%[4]。一旦出现严重出血,应停用华法林。静脉内给予维生素K(5~10mg)常可在24h内拮抗华法林作用。如果需要更快的对抗效果可给予新鲜血浆。 抗凝治疗可有效地避免血栓形成的病人发生PE。华法林或皮下肝素的抗凝治疗在第一次发生DVT的病人中应持续6个月[7~9]。伴有PE及持续DVT危险因素(恶性病变及高凝状态)的病人应终生服用华法林。2 溶栓治疗溶栓治疗已经有30多年的历史,具有肯定的疗效,但目前在许多细节问题上仍有争论,治疗方法有待不断研究和完善[10]。溶栓治疗的目的是期望完全恢复下肢静脉机能[11],包括使深静脉系统恢复通畅,且维持瓣膜功能。深静脉血栓形成后综合征(PTS)的病理过程是由于血栓机化造成瓣膜关闭不全及残余静脉血栓阻塞,阻塞段远端静脉血液回流不畅,静脉压力不断增加而产生。临床上应争取早期完全溶解原发血栓,这有利于恢复血流通畅和保持正常的瓣膜功能。3天之内(特别是24h之内)的新鲜及非闭塞性血栓是溶栓的最好适应证。溶栓药物包括尿激酶(UK),重组组织型纤溶酶原活化剂(rt-PA)。两者均是通过激活纤溶酶原,使之转变为纤溶酶来溶解血栓。由于价格的原因,UK较rt-PA更为常用。在疗效方面二者孰优孰劣尚无定论[12]。但从我们临床应用的情况看,应用rt-PA的病人之治疗效果似强于应用UK的治疗效果。给天普洛欣,中间辅以肝素抗凝。首次剂量75~100万单位,4h内输注。其后,每日应用50~70万单位,连续7~10日。rt-PA(“爱通立”,BoehringerIngelheim德国)的使用我们首先在1~2min内静脉推注10mg;然后在1h内静脉输注50mg;最后2h内继续静脉内输注40mg,总量为100mg/3h。必要时可在首次用药24h后再加用50mg。溶栓期间,PT、APTT、凝血酶时间及纤维蛋白原水平每日检测2~4次。这些检查都不能预测疗效成功与否或是否会出血,但如果发生出血却可指导治疗。溶栓结束后,应继续抗凝治疗(肝素及华法林)。虽然溶栓治疗对DVT的病人有较好的临床效果,但血栓完全溶解率极低。有资料显示髂股静脉血栓溶栓成功率只有28%[1]。其原因是由于此类病变中血栓较大,且其堵塞部位的静脉血流中断,妨碍了药物与血块的直接接触,还包括溶栓时间较晚等原因。溶栓治疗的主要并发症是导致严重出血。以下是溶栓治疗的禁忌证:大中型手术不足1个月、分娩期及产褥期、胃肠道出血及严重创伤等有可能造成严重出血的病例。出血体质、颅内病变、近期的中风(不足2个月)及颅内、脊柱手术也是溶栓治疗的禁忌证。特别要强调,高血压病人如果血压超过或等于:收缩压180mmHg(24kPa)和(或)舒张压110mmHg(14·67kPa),应禁用溶栓药物。即使此类病人的血压得到控制,应慎用溶栓治疗,并在治疗期间严密监测血压变化,必要时停止溶栓治疗。DVT病人溶栓治疗出血并发症的发生率是0~17%[1]。溶栓失败的原因包括:长段或广泛的DVT,可造成溶栓药物不能与血栓良好接触,病程过长的、陈旧的、机化血栓,溶解纤维蛋白反应不充分,过早停止溶栓药的使用。3 溶栓抗凝治疗有待解决的问题在溶栓治疗中,是否完全溶解阻塞血栓与相关症状缓解的快慢的关系一直尚无定论。虽然溶栓药物较肝素组明显改善了血栓消退,但病人临床症状的减轻方面并无明显区别,一个可能的解释是:除药物溶栓的作用外,不少病人症状体征的消退是由于侧支循环的建立而非血栓的完全消退[13]。积极溶栓治疗,尽量消除血栓,以减少瓣膜的损伤程度,从而减轻PTS后静脉返流所造成的并发症。溶栓能否消除瓣窦内的血栓,究竟对瓣膜功能恢复是有效还是无效,学术上仍有争论[14,15]。溶栓治疗后再次血栓形成,即复发问题。溶栓的成功依赖于血栓内与纤维蛋白溶解酶原相结合的纤维蛋白的数量,即与血栓形成时间有相互关系[10]。血栓超过1周时间的病人其疗效很难成功。目前,医生很难准确判定血块形成的时间,基本上仅依赖于病人症状、体征出现时间的长短,而临床上确实已发现无症状静脉血栓的病人,只要有陈旧血栓存在,或者静脉内膜的损伤已造成纤维性狭窄,就有再次血栓形成的可能,说明溶栓治疗后应长期继续抗凝治疗的重要性。溶栓治疗前是否须放置滤器?DVT溶栓治疗PE发生率是很低的,但由于有潜在发生医源性肺栓塞的可能,溶栓时绝对卧床,避免按摩挤压患肢等,可明显减少PE发生率。对已发生PE的病人,在溶栓治疗前应放置下腔静脉滤器。如在溶栓治疗过程中发生PE,这些栓子也许很快会由于持续的溶栓药物输注而溶解。我们很少对接受溶栓治疗的病人放置滤器。溶栓治疗同时是否联合应用抗凝药物?我们认为,在严密监测及避免严重出血的前提下,两者同时应用必会加强和巩固溶栓效果,已有相关报道支持这一观点[16]。在给药途径方面,全身溶栓与通过患肢末梢静脉输注两者间的比较,均显示前者的疗效优于后者,这多少与想象有所差别,但应注意到前者的剂量在试验中大大高于后者[17,18]。总之,针对DVT的治疗,应在遵循治疗原则的基础上因人而异。血栓发生部位、类型,以及病人的个体因素等等方面均对疗效有着重要的影响。如何看待溶栓治疗过程中潜在的医源性肺栓塞的可能及严重出血的危险?到底什么类型的DVT病人对溶栓治疗最有效?何种溶栓药物及剂量最有效?溶栓治疗是否可避免PTS?诸多疑问需要更多、更严谨、更科学的临床研究来解答。本刊对此病进行专题讨论很有必要,建议适当时间可以召开专题研讨会,做更深入的讨论,以规范诊疗方法。
终于在9月整个地区超过1000盒。虽然这个数字看起来不多,但是当时整个地区一个月行PTCA病人数不到30病人情况下,我已很有成就感了
,我拜访相关人员,搜集到药事委员会有哪些成员,替代的具体经过,分管院长等相关信息,在主管及大区经理等大力帮助下,成功的再用速碧林取代了克赛。为速碧林在整个地区低分子肝素排名中占据第一名打下了基础
中山医院心内科是个很特殊的地方,科室大,人员多。带组医生对床位医生的用药约束却比较弱。因此,床位医生选择何种药物就要靠代表各个击破。50多个床位医生中,95%以上是临床轮转的研究生和外地来的进修医生。并且每个月都有20%以上的更新率。两年来我常常觉得很辛苦,为了维持速碧林在中山心内科的主导用药地位,我必须让这50多个医生中超过半数的人认可“速碧林在抗凝疗效上绝不亚于克赛等竞争产品,但是在注射部位局部的耐受性上是显著优于其他竞争产品”的这一观念,从而把速碧林作为不稳定心绞痛和非Q波心梗患者的临床首选用药。因此在心内科投入了大量的时间和精力,并且同时还要做好其他的科室和医院,所以经常让我觉得不堪重负。但是,从接手中山第一天起,无论境遇怎样,心底深处始终有个坚定的声音告诉我:“坚持下去!中山我称王!”每一天,迎着灿烂的朝阳出门,伴着满天的繁星回家。转眼已过两年,汗水洒处,一份份快乐与感动滋润了心田。除了速碧林在心内科始终维持的主导用药地位外,每当能给进修医生带来一些工作,生活,学习上的帮助;每当与刚上临床的年轻研究生交流人生的感悟,帮助他们不断调整心
在2007年全球畅销药物前50强排名中,入围产品的总销售收入排名前5位的制药企业依次为辉瑞、赛诺菲-安万特、罗氏、阿斯利康和葛兰素史克。
在2007年全球畅销药物前50强排行榜中,辉瑞的产品占了5只。这些药物的总销售收入高达251.59亿美元,名列第一。除了立普妥和抗高血压药氨氯地平(Amlodipine,络活喜,Norvasc)之外,还有抗关节炎药塞来昔布(Celecoxib,西乐葆,Celebrex)、抗癫痫药普瑞巴林(Pregabalin,Lyrica)和勃起功能障碍(ED)治疗药西地那非(Sidenafil,万艾可,Viagra)。
赛诺菲-安万特名列第二,有6只产品进入全球畅销药物50强排行榜,入围产品的销售收入总计达170.36亿美元。抗血栓药依诺肝素钠(Enoxaparin,Lovenox)是该公司表现最好的品种,达到38亿美元的销售额,同比增长了18.4%;抗糖尿病药甘精胰岛素(InsulinGlargine,来得时,Lantus)实现销售额30亿美元,大幅增长了36.4%;乳腺癌、非小细胞肺癌治疗药多西他赛(Docetaxel,泰索帝,Taxotere)销售额达27.06亿美元,同比增长了17.1%。
罗氏名列第三,有5只产品进入了全球畅销药物前50强排行榜,入围产品的总销售收入达162.3亿美元。3只单抗类抗肿瘤药继续保持快速增长的势头:利妥昔单抗(Rituximab,MabThera)销售同比增长了24%,乳癌治疗药曲妥珠单抗(Trastuzumab,赫赛汀,Herceptin)增长了34%,结直肠癌治疗药贝伐单抗(Bevacizumab,阿瓦斯丁,Avastin)增长了48%。抗流感药物奥司他韦(Oseltamivir,达菲,Tamiflu)销量下滑,2007年销售为17.4亿美元,下降了19%。血液调节药倍他依泊汀(NeoRecormon)则继续下降7%,销售额为16.9亿美元。
阿斯利康名列第四,有4只产品进入了全球畅销药物前50强排行榜,入围产品的总销售收入达137.69亿美元。除了抗溃疡药Nexium以外,还包括:抗精神病药富马酸喹硫平(Quetiapinefumarate,Seroquel)、降血脂药罗伐他汀(Rosuvastatin,Crestor)和乳腺癌治疗药阿那曲唑(Anastrozole,瑞宁得,Arimidex)。
葛兰素史克的入围产品也有4只,总销售收入为135.1亿美元,位列第五。除了排在第四位的抗哮喘药Advair/Seretide外,其余产品均排名靠后。其中包括2型糖尿病治疗药罗格列酮(Rosiglitazone,文迪雅,Avandia/Avandamet)、癫痫及双相情感障碍治疗药拉莫三嗪(Lamotrigine,Lamictal)和疱疹治疗药伐昔洛韦(Valacyclovir,Valtrex)。
其一是抗凝血剂。陶剑虹指出这是目前全球一个有待大量满足的医疗需求,例如,在美国每年有600万的人因患有深静脉血栓而住院;据IMS统计,2008年全球血小板凝集抑制剂市场规模达136.33亿美元,同比增长了13.90%,列全球处方药市场15大畅销治疗类别的第十一位。目前,中国65岁以上的老龄人口已超过1亿;2015年,老龄人口将达到2亿;到2040年,将突破4亿。而据统计,65岁以上人口心脑血管血栓的患病率在20%左右。整个社会对于抗血栓药物的需求庞大。
抗凝剂快速增长的动力主要源于创新。从最早的普通肝素到华法林、低分子肝素,再到直接凝血酶抑制剂和近来比较热门的Xa因子抑制剂,这一领域的创新不曾止步。2008年,全球抗凝血药市场规模62亿美元,到2014年可以达到91亿美元,其中低分子肝素的市场总量从45亿美元下降到28.5亿美元,取而代之的将是Xa因子抑制剂从3.25亿美元成长到29亿美元的规模。其中拜耳和强生公司联合开发的Xarelto预计在上市当年就可创出1.2亿美元的销售收入。是十分有潜力的“准重磅炸弹药物”。
实际上在这一用药领域中国的国产品竞争优势还不明显,以低分子肝素钠(依诺肝素钠)为例,法国赛诺菲安万特的低分子肝素钠市场份额超过60%;而低分子肝素钙的医院市场中,葛兰素史克的“速碧林”占有优势地位,2008年占据了六成以上的市场份额;而以氯吡格雷为例,目前赛诺菲安万特的波立维更是一枝独秀。
速碧林
Fraxiparine
2003年,Fraxiparine的销售额为3亿1900万欧元
2008年全球销售 2.26亿英镑,4.18亿美元
2009年全球销售 2.29亿英镑,3.57亿美元
2010年全球销售 2.22亿英镑,3.44亿美元
2011年全球销售 2.34亿英镑
看来速碧林的销量很稳定。
http://bbs.seedit.com/thread-1344956-1-1.html
一周前到医院验血,孕酮比较低,医生让住院保胎,每天一针黄体酮和两针“低分子肝素钙”。打针的护士说现在医院里很多先兆流产的都在打这个“低分子肝素钙”,是肚皮上注射,可以防止形成血栓。
今天医生说这个针一直可以打到12周,这里有姐妹打过这个针吗?
打低分子肝素,妊娠期血栓
我老婆已经打一周了,她得了静脉血栓,医生说至少要打六个月,会不会有危险和负作用啊,希望有经验的妈妈多联系,QQ:7818326,她的预产期:2012年6月22日,
已经打了40多天了..现在出现红肿...而且还有结块...
很难消下去了..红肿的地方还痒..
现在真不知道怎么办才好..
有姐妹有这种情况吗?
我也是怀孕一个多月发现右小腿静脉血栓,一直注射低分子肝素钙0.4毫克,每天2次。已经打了一个半月了,我这里的医生说抗凝最少得用三个月,在网上搜了很多资料都说早孕期可以用,但是心里还是害怕啊,还有更多用孕期用了低分子肝素钙的姐妹请互相联系一下啊,我的QQ号:65949449
我老公的 妹妹打这个保胎的,是肝素钠还是肝素钙我不是很清楚,打到三个月,现在宝宝生出来很健康
我也打,打的是速碧林,一针68.5,每天一针,已经打了20天了,好像要打到怀孕90天,安全以后就停了!
我也开始打这个针了,因为怀孕引起的小腿静脉血栓。我打的是胳膊啊,打肚皮我害怕。我是在解放军总医院打的。
低分子肝素的副作用
所患疾病:狼疮抗凝物
病情描述(发病时间、主要症状、就诊医院等):
狼疮抗凝物 阳性
曾经治疗情况和效果:
低分子肝素钙12H/支,阿司匹林50MG/天,强的松1片/天,丹参川穹嗪
想得到怎样的帮助:
注射低分子肝素有何副作用,刚开始的半个月无淤青无痛无痒,现在注射部位数小时后发红发痒,是正常的么?有时候奇痒难忍,有什么办法可以缓解?有朋友用速碧林,进口药是否副作用和药效好一点?
发表于 2012-08-05 18:22:04
上面没有说明白,我是之前胎停育过,这次怀孕查出了狼疮抗凝物阳性,在大夫指导下用肝素保胎,出现了上述情况
2008~2009年,我科采用低分子肝素治疗系统性红斑狼疮指端坏疽患者2例。根据对上述2例患者的观察,我们认为:严重的雷诺氏现象、手足部位的青紫斑、躯干、四肢呈网状的红斑/青斑等临床表现有助于判断系统性红斑狼疮的外周血管病变严重程度;低分子肝素对于纠正凝血状态、防止指端坏疽的发生具有较肯定的疗效;外周血管病变较重,特别是累及指端部位的患者,需要早期应用低分子肝素进行干预。
 爱华网
爱华网