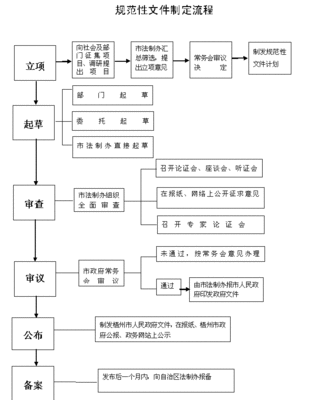
根据药品GMP规定,每批产品均应当有相应的批生产记录,可以追溯该产品的生产历史以及与质量相关的情况。药厂QA的另外一项工作就是审核批生产记录,审核记录的时候,该记录应该和批准的工艺规程一致,这里熟悉每一步的工艺流程也是一项重要的工作。
作为药厂QA认识批生产记录尤为重要,这里我所说的批生产记录是一个总称,既是包括药品生产一切的记录体现,下面是我对批生产记录的认识(存在局限性,还望各位见谅):
首先,药厂生产的每一批药品都要相应的记录,这个记录包括从原材料的处理到外包装的成品入库的每一步,即是体现了每一步的相应的规程,在整个生产过程中的每一个步骤有相应的记录表格,根据生产的实际情况将记录填写在表格上,在操作结束后,应当有生产操作员确认并签名和记录下时间。

其次,批生产记录的内容应该包括以下几点:
1,药品的品名、规格、批号。
2,生产以及中间工序开始到结束的日期和时间。
3,每一个生产工序的都要负责人,即班长签字。
4,生产步骤操作人员的签名;还应当有复核人员的签名。
5,每一步骤的所需的原辅料的批号以及实际称量的数量、使用量、消耗量和回收量的记录。
6,在记录上填写相关的工艺参数和控制范围,以及主要生产设备的编号。
7,不同生产工序结束后所得产量记录和物料平衡计算。
8,现场监理人员即药厂QA在监控开始和结束的签字,当然也包括清场合格证和生产许可证的发放。
最后,每一个工序的负责人将该工序填写好的记录交到生产负责人处,进行总汇,再由负责人填写生产总汇表,然后所有的表格进行装订,进行检查复核后交到质量部审核。
药厂QA对批生产记录的认识能够帮助QA对记录审核,对记录的审核一定要认真,不放过任何一个疑惑点和错误点,在下一篇博文中我会分享一些审核经验,当然毕竟我只在小药厂呆过,很多东西都有不足,望请各位谅解。
 爱华网
爱华网