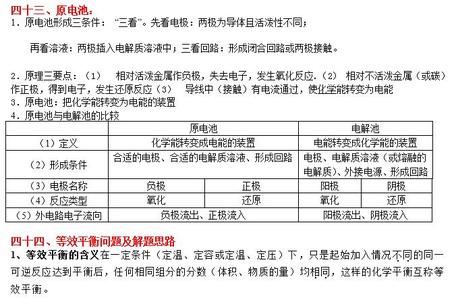
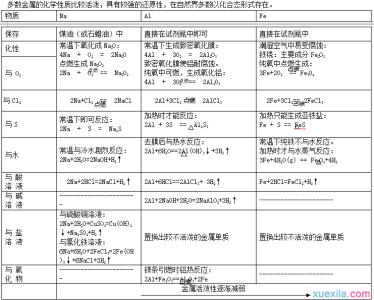
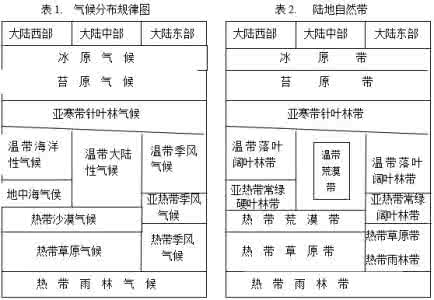
化学知识让我们能直观了解到物质变化的过程及结果。下面是小编为大家整理的高中化学会考知识点复习,希望对大家有所帮助。
高中化学会考知识点复习(一)1.中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准掖;先用待测液润洗后再移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点。
2.焰色反应实验时,每做一次,铂丝应先沾上稀盐酸放在火焰上灼烧到无色时,再做下一次实验。
3.用H2还原CuO时,先通H2流,后加热CuO,反应完毕后先撤酒精灯,冷却后再停止通H2。
4.配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用胶头滴管加水至刻度线。
5.安装发生装置时,遵循的原则是:自下而上,先左后右或先下后上,先左后右。
6.浓H2SO4不慎洒到皮肤上,先迅速用布擦干,再用水冲洗,最后再涂上3%一5%的 NaHCO3溶液。沾上其他酸时,先水洗,后涂 NaHCO3溶液。
高中化学会考知识点复习(二)了解钠、铝、铁、铜等金属分别与氧气、水、酸、碱、盐等物质反应的情况,了解其共性和个性 。
(1)与纯氧气反应:
①.常温:钠变质生成白色氧化钠,铝表面生成致密的氧化物薄膜保护内部金属不再反应,铁、铜稳定存在。
②.加热:白色钠燃烧发出黄光生成淡黄色的过氧化钠,熔化的铝被白色氧化膜包裹不会滴落,白色铁丝燃烧产生耀眼的白光,有黑色颗粒物(Fe3O4)落下,紫红色的铜加热变成黑色的氧化铜。
说明:钠与氧气反应温度不同产物不同;铁与氧气反应的产物随接触面积、量的多少、温度高低有关。
(2)与水的反应
①.常温:只有钠能与水反应;铝、铁、铜不与水反应。
ⅰ、钠跟水的反应的化学方程式:2Na + 2H2O=2NaOH + H2↑ ;离子方程式:2Na + 2H2O=2Na+ + 2OH- + H2↑
ⅱ、钠跟水的反应的现象:概括为“浮、熔、游、响、红”五个字来记忆” 。
ⅲ、钠跟水的反应的现象的解释:浮:钠的密度比水小;熔:反应放热,钠熔点低熔化成小球;游:反应产生气体;响:反应剧烈 ;红:生成NaOH,酚酞遇碱变红 。
高中化学会考知识点复习(三)1.加热试管时,应先均匀加热后局部加热。
2.用排水法收集气体时,先拿出导管后撤酒精灯。
3.制取气体时,先检验气密性后装药品。
4.收集气体时,先排净装置中的空气后再收集。 5.稀释浓硫酸时,烧杯中先装一定量蒸馏水后再沿器壁缓慢注入浓硫酸。 6.点燃H2、CH4、C2H4、C2H2等可燃气体时,先检验纯度再点燃。
7.检验卤化烃分子的卤元素时,在水解后的溶液中先加稀HNO3再加AgNO3溶液。
8.检验NH3(用红色石蕊试纸)、Cl2(用淀粉KI试纸)、H2S[用Pb(Ac)2试纸]等气体时,先用蒸馏水润湿试纸后再与气体接触。
9.做固体药品之间的反应实验时,先单独研碎后再混合。

 爱华网
爱华网